|
定量NMRを用いた加工食品中の食品添加物分析
日本大学生物資源科学部 食品生命学科
専任講師 大槻 崇 1.はじめに核磁気共鳴(NMR)は、スペクトル上の共鳴シグナルの化学シフトやシグナルの多重度、分裂幅、面積強度などを通じて測定対象物質に関する多種多様な構造情報を与える。またNMRは測定対象物質を非破壊で分析できることから、天然化合物、化学合成品など様々な有機化合物の構造決定等における重要なツールとして広く使用されている。さらに近年では、超伝導マグネットの高磁場化、プローブの改良などに伴い、NMRは定性にとどまらず実用的な定量分析装置としても認知されつつある。このNMRを使った定量法、いわゆる定量NMRは、①測定対象物質と同一の定量用標品が不要、②定量のための検量線が不要、③計量計測トレーサビリティを確保した測定対象物質の含量の算出が可能など、分析の効率性、迅速性、得られる定量値の信頼性の向上に大きく貢献できる新たな定量法として注目を集めている1,2)。また、このような特長を背景に、定量NMRは生薬指標成分や食品添加物の定量用試薬(標品)の純度分析法など、公的な分析法への採用も進んでいる3-6)。 2.加工食品中の食品添加物分析10)日本では食品添加物の安全性や品質を確保する目的で、食品添加物の性状、含量(純度)などの成分規格や食品添加物を使用できる食品の種類、使用量などの使用基準などが設定され、これらの規格、基準が守られているかを監視するための分析法が別途規定されている。このうち、食品中の使用量を試験するための分析法いわゆる「食品中の食品添加物分析法」では、主に液体クロマトグラフ等の機器が用いられるが、定量には測定対象物質と同一かつ純度が正確な定量用標品が必要である。しかし、計量学的に妥当な手順によって純度が算出された認証標準物質(CRM)は非常に少ない。このため、液体クロマトグラフィー等の相対定量法では、試薬メーカーの標準品が一般的に利用されている。しかし、この純度は自社規格により保証されたもの、すなわち計量学的に正確とは言えず、結果として定量値の信頼性が損なわれる可能性を否定できない。また、食品や測定対象物質によっては煩雑な前処理や低回収率等の問題点もあり、その改善が望まれている。 1H-qNMRは検出手法が測定対象物質の吸光や蛍光などの物性に依存しない測定法であるため、CRMのような標準物質を内標準物質として用いることにより、様々な有機化合物に対して分析値の信頼性を確保した絶対定量が可能である。また、測定対象物質の定量用シグナルが、その分子内の他のシグナルや夾雑物に由来するシグナルと十分に分離されていれば、測定対象物質の精確な定量が可能である。このため、多段階のクリーンアップや誘導体化等の前処理が不要となる可能性がある。従って、1H-qNMRは迅速性、簡便性、選択性の面で従来法よりも優れた分析法と言える。またこのような特長をもつ1H-qNMRの食品添加物分析への応用は、食品添加物の使用基準の評価における分析値の計量計測トレーサビリティの確保、ひいては国民の要望が高い食品添加物の安全の一層の確保に貢献できると考えられる。 3.1H-qNMRを用いた食品中のデヒドロ酢酸ナトリウム分析11)デヒドロ酢酸ナトリウムは、保存料として使用が認められた食品添加物であり、日本ではバター、チーズ、マーガリンへの使用基準が設けられている。 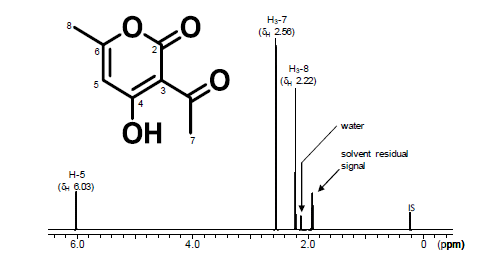 図1.デヒドロ酢酸の化学構造および1H-NMRスペクトル 測定溶媒:重アセトニトリル 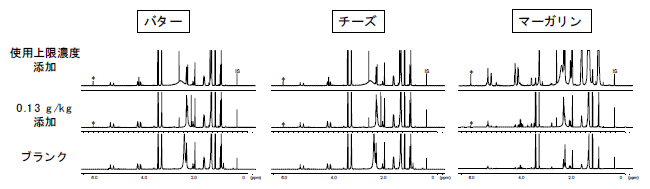 図2.デヒドロ酢酸を添加した各食品の1H-NMRスペクトル *:定量用シグナル,IS:内標準物質(1,4-BTMSB-d4),測定溶媒:重アセトニトリル
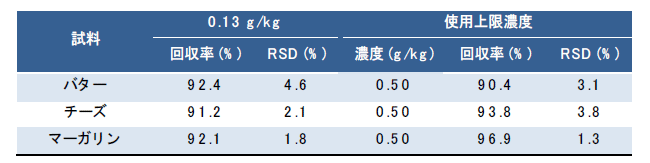
表1.各食品における添加回収試験結果(n=3)
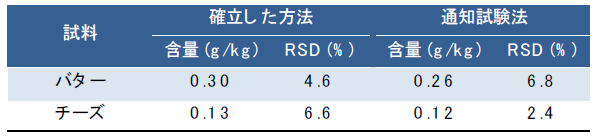
 次に市販食品分析への本法の有用性を明らかにするため、デヒドロ酢酸ナトリウムの使用が表示された2種の加工食品(バター,マーガリン)について分析し(図3)、得られた結果を通知試験法12)(試験溶液の調製:水蒸気蒸留,分析:液体クロマトグラフィー)と比較した。その結果、両試料ともに本法と通知法により得られたデヒドロ酢酸ナトリウムの測定値はほぼ同等であり、本法は通知法と同程度に正確な定量結果を与えることが示された(表2)。 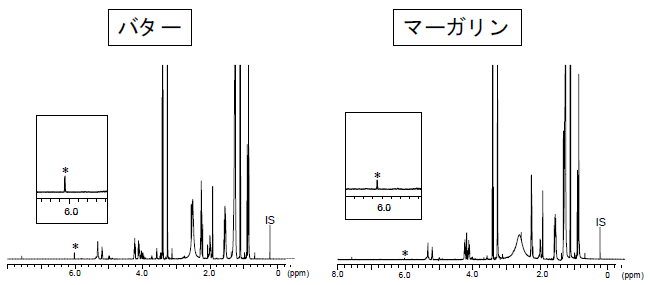 図3.デヒドロ酢酸ナトリウムの使用が表示された食品の1H-NMRスペクトル *:定量用シグナル,IS:内標準物質(1,4-BTMSB-d4),測定溶媒:重アセトニトリル
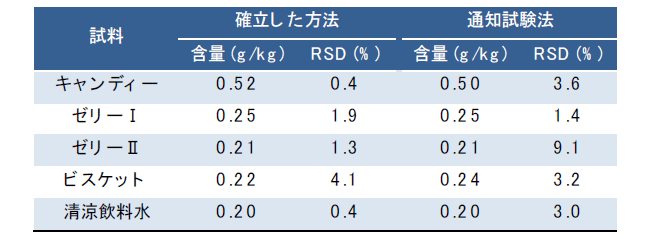
表2.2つの方法により算出された各食品中のデヒドロ酢酸ナトリウム含量(n=3)
 4.1H-qNMRを用いた食品中のアセスルファムカリウム分析13)アセスルファムカリウムは甘味料の1つであり、日本では菓子、漬け物、果実酒、清涼飲料水のみならず「その他の食品」に対しても使用基準が設けられており、幅広い食品に対して使用が可能な食品添加物である。このアセスルファムカリウムを対象とした1H-qNMRを用いた分析法を確立するにあたり、試験溶液は、デヒドロ酢酸ナトリウム分析法の前処理の一部を変更して調製した。 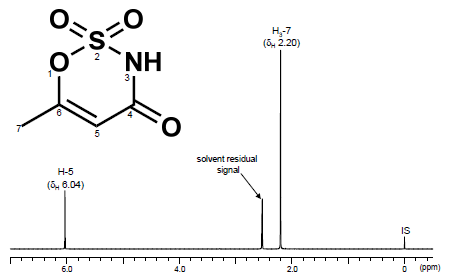 図4.アセスルファムの化学構造および1H-NMRスペクトル 測定溶媒:重ジメチルスルホキシド 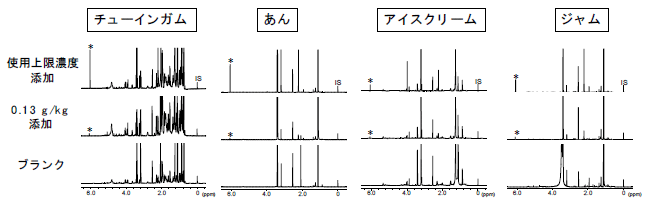 図5.アセスルファムを添加した各食品の1H-NMRスペクトル *:定量用シグナル,IS:内標準物質(DSS-d6),測定溶媒:重ジメチルスルホキシド
表3.各食品における添加回収試験結果(n=3)
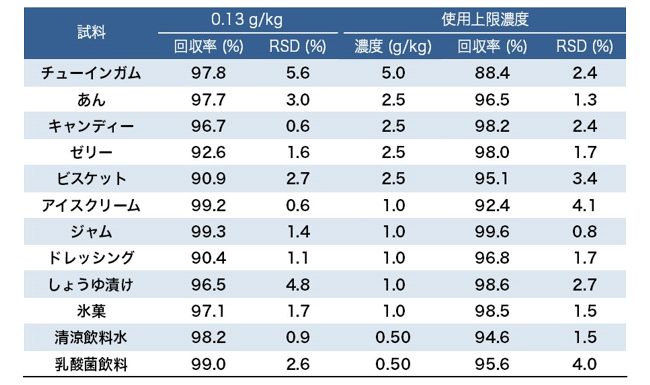 また、アセスルファムカリウムを含有する加工食品への本法の適用性を明らかにするため、 その使用が表示された5種の加工食品を分析し(図6)、得られた定量値を通知試験法14)(試験溶液の調製:透析,分析:液体クロマトグラフィー)と比較した。その結果、すべての試料で本法と通知試験法の結果はほぼ同等であり、本法は通知試験法と同程度に正確な定量結果を与えることが判明した(表4)。なお、本法は、分析時間が1検体あたり60分程度と通知試験法(デヒドロ酢酸分析: 125分,アセスルファムカリウム分析:25~49時間)に比べ大幅に短縮できた。 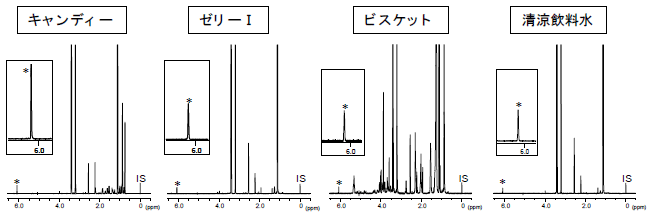 図6.アセスルファムカリウムの使用が表示された食品の1H-NMRスペクトル *:定量用シグナル,IS:内標準物質(DSS-d6),測定溶媒:重ジメチルスルホキシド
表4.2つの方法により算出された各食品中のアセスルファムカリウム含量(n=3)
 5.まとめ本稿では1H-qNMRによる加工食品中の食品添加物分析を例に、定量NMRのアプリケーションを述べさせていただいた。現在の食品関連物質の分析では、クロマトグラフィーが主流であり、1H-qNMRが感度や測定コストなどの点でやや劣ることは否めない。しかし、クロマトグラフィーにも定量用標品や分離機構の限界などの問題が存在する。1H-qNMRは迅速性や得られる定量値の信頼性の向上などに資するだけではなく、定量用標品の入手が困難な測定対象物質についても、その化学シフトさえわかれば、1H-qNMRで絶対定量が可能となるなど非常に優れた特長を有している。また、1H-qNMRはシグナルの分離機構がクロマトグラフィーとは全く異なるため、クロマトグラフィーで分離が困難な測定対象物質についても本法での定量の可能性が期待できる。どちらの分析法が良いというわけではなく、分析法の利点と分析の目的に応じて使い分け、時には相補的に利用することにより、様々な分野で利用されている1H-qNMRを含む定量NMR15-17)の適用範囲は更に拡大するだろう。 参考文献1 N. Sugimoto, M. Tahara, T. Suematsu & T. Miura: Food Hyg. Saf. Sci., 53, J-228 (2012). 2 合田幸広:医薬品医療機器レギュラトリーサイエンス,44,753 (2013). 3 第十七改正日本薬局方(厚生労働省) 4 平成23年厚生労働省告示第307号(2011)“食品,添加物等の規格基準の一部を改正する件” 平成23年8月31日. 5 平成25年厚生労働省告示第45号(2013)“食品,添加物等の規格基準の一部を改正する件” 平成25年3月12日. 6 平成25年厚生労働省告示第268号(2013)“食品,添加物等の規格基準の一部を改正する件”,平成25年8月6日. 7 T. Ohtsuki, K. Sato, N. Sugimoto, H. Akiyama & Y. Kawamura: Anal. Chim. Acta, 734, 54 (2012). 8 T. Ohtsuki, K. Sato, N. Sugimoto, H. Akiyama & Y. Kawamura: Talanta, 99, 342 (2012). 9 T. Ohtsuki, A.Tada, M. Tahara, T. Suematsu & N. Sugimoto: Applications of NMR Spectroscopy, 4, 222 (2016). 10 大槻崇:化学と生物,52,622 (2014) 11 T. Ohtsuki, K. Sato, N. Sugimoto & H. Akiyama: Food Chem., 141, 1322 (2013). 12 厚生労働省医薬食品局食品安全部基準審査課長通知 “「食品中の食品添加物分析法」の改正について” 平成22年5月28日,食安基発0528第3号(2010). 13 T. Ohtsuki, K. Sato, Y. Abe, N. Sugimoto & H. Akiyama: Talanta, 131, 712 (2015). 14 厚生労働省医薬局食品保健部基準課長通知 “食品中のアセスルファムカリウム分析法について” 平成13年12月28日,食基発第58号(2001). 15 Y. Jadeja, B. Chomal, M. Patel, H. Jebaliya, R. Khunt & A. Shah: Magn. Reson. Chem.,55, 634 (2017) 16 G. Assemat, F. Dubocq, S. Balayssac, C. Lamoureux, M. Malet-Martino & V. Gilard: Forensic Sci Int., 279, 88 (2017). 17 R. Watanabe, C. Sugai, T. Yamazaki, R.Matsushima, H. Uchida, M. Matsumiya, A. Takatsu & T. Suzuki: Toxins, 8, 294 (2016). 略歴大槻崇 (おおつき たかし) 略歴 サナテックメールマガジンへのご意見・ご感想を〈e-magazine@mac.or.jp〉までお寄せください。 |
| Copyright (C) Food Analysis Technology Center SUNATEC. All Rights Reserved. |

