|
マリンカロテノイドの生体内代謝と生物活性(機能性)
京都大学大学院 農学研究科 准教授 真鍋 祐樹 1. はじめにカロテノイドは分子内に8つのイソプレン構造を有するテトラテルペンである。2つの環状構造を鎖状構造が接続する化学構造を有しており、長く共役する炭素二重結合のために、通常、黄色から赤色を呈する。最も単純な構造を有しているβ-カロテン(1)は両端に修飾を受けていないβ環(非修飾β環)を有しており、片側の環構造が非修飾ε環に代わるとα-カロテン(2)、β-カロテンのC-3位がヒドロキシ基で修飾されるとβ-クリプトキサンチン(3)というように、様々な化学構造のカロテノイドが知られている(図1、各カロテノイド名の後に付記した数字は図1中の番号を指示している。以下同様。)。なかでも非修飾β環をひとつでも有するカロテノイドはヒト体内でビタミンAに代謝変換され得るため、プロビタミンAに分類され、食事中ではβ-カロテン、α-カロテン、β-クリプトキサンチンの3種類が特に重要と考えられている。さらに、ルテイン(4)やゼアキサンチン(5)などは機能性表示食品の関与成分としても利用されており、食用色素から栄養素、機能性食品成分に至るまで、カロテノイドは食に関わる様々な用途で有効活用されている。 海産物に特徴的に含まれるカロテノイド(マリンカロテノイド)は、野菜や果物などの海産物以外の食材に含まれるカロテノイドと比べて特徴的な化学構造を有していることが多く、新規食品機能性成分としての有効利用が期待されている。実際、エビやカニなどの甲殻類に含まれるアスタキサンチン(6)や、ワカメやコンブなどの褐藻類に含まれるフコキサンチン(7)に強い抗酸化作用1と抗肥満作用2が見出され、機能性表示食品の関与成分として社会実装が実現している。しかしながら、その希少性のために生物活性の評価が進んでいないマリンカロテノイドも数多く残されている。筆者らは抗炎症作用を中心にマリンカロテノイドの生物活性の評価を進めており、そのなかでクビレズタ(海ぶどう)に含まれるシフォナキサンチン(8)やマボヤなどに含まれるハロシンチアキサンチン(9)に強い抗炎症作用を見出した。さらにこれらのマリンカロテノイドが生体内において、より強い活性を示す化学構造へ代謝変換され得ることを見出したため、本稿で紹介する。
 図1. マリンカロテノイドの化学構造の例 カロテノイド名の後に付記した数字は本文中の番号と対応している。
2. シフォナキサンチンの脱水素化反応(デヒドロ体の生成)シフォナキサンチンは陸上植物が光合成色素として有するルテインの類縁体であり、ミルやクビレズタなどの一部の緑藻の光合成色素のひとつである。筆者らは、シフォナキサンチンがマウス前駆脂肪細胞株3T3-L1の脂肪細胞への分化を強く抑制することを見出し、さらに、その経口投与によって、肥満併発二型糖尿病モデルマウスKK-Ayの腸間膜脂肪組織重量が減少することを報告している3。このとき、マウス体内から、シフォナキサンチンのみならず、食餌に含まれていないカロテノイドが3種類検出され、その後のLC/MS解析およびNMR解析、CD解析の結果、シフォナキサンチンのジデヒドロ体2種類とテトラデヒドロ体1種類と同定された(図2)4。また、培養細胞を用いた検討によって、これらのデヒドロ体が元のシフォナキサンチンよりも強い抗炎症作用を示すことが明らかになった4。さらに、シフォナキサンチンを摂食させたマウスの血漿や各種臓器を調べたところ、ほとんどの臓器においてシフォナキサンチンよりもデヒドロ体の方が多く蓄積していた5。これらの実験結果より、デヒドロ体への代謝変換が個体レベルにおけるシフォナキサンチンの機能性の発現に重要であると推察される。肝臓S9画分(肝臓ホモジネートを遠心分離して得られ、様々な薬物代謝酵素が含まれる画分)を用いた比較ではあるが、マウスとラットではデヒドロ体の生成量が異なるため4、シフォナキサンチンの機能性を個体レベルで評価する際には、評価に用いる動物種にも注意が必要といえる。また、ヒト肝臓S9画分やHepaRG細胞(薬物代謝の研究に利用されるヒト肝臓由来細胞)においてもシフォナキサンチンのデヒドロ体への代謝変換(脱水素化反応)を確認しており4、ヒトにおいてもデヒドロ体の生成を介したシフォナキサンチンの機能性が期待される。
 図2. シフォナキサンチンのデヒドロ体とその抗炎症作用(参考文献4より一部改変) グラム陽性細菌の細胞膜成分を模倣したトリアシルリポペプチドを用い、ヒト単球様THP1細胞またはマウスマクロファージ様RAW264細胞に炎症応答を誘導した。THP1細胞ではインターフェロン調節因子(IRF)の転写活性化レベルをレポータージーンアッセイを用いて評価した。また、カロテノイドの濃度は1.0 μMとした。RAW264細胞では培養上清に放出された一酸化窒素量を炎症応答の指標として評価した。Unstimは炎症応答を誘導していないコントロール、Contはカロテノイドで処理せずに炎症応答を誘導したコントロールを表す。
3. ハロシンチアキサンチンのシス-トランス異性化反応(シス体の生成)ハロシンチアキサンチンは、フコキサンチンがマボヤによって代謝変換されたカロテノイドである。これまでに抗炎症作用6やがん細胞に対するアポトーシス誘導作用7が報告されているが、個体レベルにおけるハロシンチアキサンチンの生物活性を評価した例はなく、経口摂取したハロシンチアキサンチンが消化管から吸収されるかどうか明らかではなかった。そこで精製したハロシンチアキサンチンをマウスに経口投与し、一定時間後の血漿カロテノイド組成を調べたところ、投与したall-trans型ハロシンチアキサンチンが確かに検出されるものの、投与6および9時間後では9’-cis型がall-trans型よりも多く検出された(図3)8。また、13’-cis型ハロシンチアキサンチンも投与6時間後まで時間経過と共に増加していた。肝臓においても同様の傾向が認められたが、小腸内容物では投与9時間後にようやく9’-cis型がall-trans型と同程度になるなど、9’-cis型の増加が血漿や肝臓よりも遅れていた。アスタキサンチンではcis型の方がall-trans型よりも消化管吸収性が良いとの研究報告があるが9、このハロシンチアキサンチン投与実験の結果は、all-trans型ハロシンチアキサンチンが消化管から吸収され、生体内で9’-cis型に異性化されたと考える方が自然であろう。現在、マウスの肝臓を中心にカロテノイド異性化酵素の探索を進めている。また、アスタキサンチンやフコキサンチンではcis型の方が強い生物活性を示すとの報告があるため10, 11、9’-cis型や13’-cis型ハロシンチアキサンチンの抗炎症作用にも興味がもたれる。
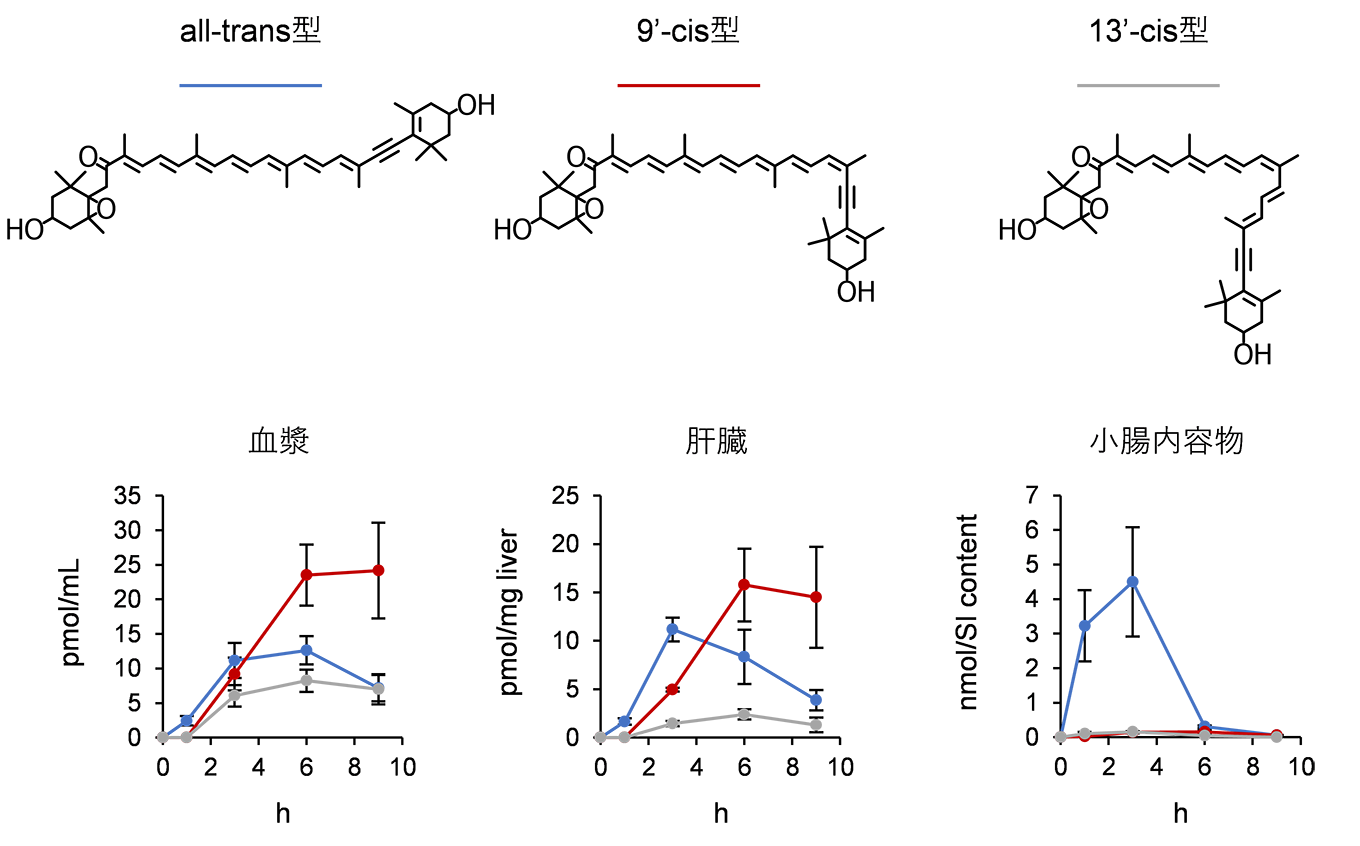 図3. 血漿および肝臓、小腸内容物中のハロシンチアキサンチンの濃度推移 (参考文献8より一部改変) オリーブオイルに溶解したall-trans型ハロシンチアキサンチンを5 mg/kg body weightとなるようにICRマウスに経口投与した。投与1、3、6、9時間後にそれぞれ解剖する群(n = 4)を設け、血漿、肝臓、小腸内容物のカロテノイド組成をHPLCを用いて解析した。SIは小腸を表す。
4. おわりに本稿では脱水素化反応とシス-トランス異性化反応を取り上げたが、マリンカロテノイドの生体内代謝には、ウニ可食部の色素であるエキネノン(10)のビタミンAへの代謝6、ヤマトシジミに含まれるペリジニン(11)やフコキサンチンの脂肪酸エステル化12, 13などが報告されている。カロテノイドは生体内で代謝変換を受けることによって、その生物活性が変化し得る。すなわち、ヒトにおける有効利用を考える上では、摂取したカロテノイドのみならず、代謝産物の同定とそれぞれの生物活性の評価が不可欠といえる。また、代謝活性には遺伝的背景や生活習慣などの環境要因に基づく個人差が存在する可能性が高く、この点を踏まえた研究も求められる。代謝に関わる酵素群を同定し、その発現や機能の多様性を明らかにすることは、マリンカロテノイドの機能性発現機構を理解し、将来的に精密な食品機能学的応用へとつなげる上で極めて重要であろう。
謝辞本研究は現所属の京都大学大学院農学研究科応用生物科学専攻海洋生物生産利用学分野にて進めたものです。サポートしてくださったスタッフや学生の皆様に感謝いたします。また、ハロシンチアキサンチンをご恵与くださった一般財団法人生産開発科学研究所の眞岡孝至博士、日本薬品株式会社の和田竜哉さまに深く御礼申し上げます。本研究はJSPS科研費JP18K14406、21K05487、24K08745、生産開発科学研究所学術奨励資金の助成を受けたものです。 参考文献
略歴
真鍋 祐樹
2012年3月京都大学大学院農学研究科博士前期課程修了。2013年4月より日本学術振興会特別研究員(DC2)を経て、2014年2月に京都大学大学院農学研究科応用生物科学専攻の助教に着任。2020年3月に博士(農学)取得。2025年10月より同准教授、現在に至る。主な研究テーマは、カロテノイドの消化管吸収メカニズムや生体内代謝変換の解明、抗炎症作用を有する食品成分の探索と作用メカニズムの解明、効率的な探索手法の開発。 サナテックメールマガジンへのご意見・ご感想を〈e-magazine@mac.or.jp〉までお寄せください。 |
| Copyright (C) Food Analysis Technology Center SUNATEC. All Rights Reserved. |


