|
カンピロバクター食中毒の予防対策構築のための定量的リスク評価
神戸学院大学 栄養学部 講師 伊藤 智 1.はじめに食中毒統計調査(厚生労働省)によると、カンピロバクター食中毒は年間を通じて発生し、細菌性食中毒の中では、平成15年以降、毎年、最も発生届出件数が多く、生や加熱不十分な鶏肉の喫食や調理段階の二次汚染による食中毒が依然として発生している。カンピロバクター食中毒の潜伏期間は1~7日間と比較的長く、比較的少量の菌数でも感染が成立する。予後は一般的に良好であるが、筋肉を動かす運動神経が障害されるギラン・バレー症候群など重症化することもある。 カンピロバクター属菌の食品への汚染経路として、生産段階において、カンピロバクター属菌を保菌する家畜・家きんのとさつ・解体時に、体表に付着していた菌が食肉等に付着、または消化管が切れて内容物が食肉等に付着して汚染する。調理・消費段階においては汚染された食肉等が生もしくは加熱不十分な状態で提供、消費されること、または、汚染された食材と接触した手指もしくはまな板や箸などの調理器具などを介して他の食品も汚染され、その食品が提供、消費されることにより、食中毒を引き起こす。 カンピロバクター属菌は環境中に広く存在し、鶏舎等への侵入経路も複雑であることから、現時点で有効な管理手法が必ずしも明確になっておらず、生産段階において菌量を抑制することが難しいと考えられている。したがって、カンピロバクター食中毒を予防するためには、フードチェーン下流の調理・消費段階での加熱処理後の生残・死滅菌数や調理操作時の器具を介した伝播率等の定量的リスク評価データをベースにしたリスク管理戦略が必要となる。また、カンピロバクター食中毒は食品中の微量の菌の存在によって発生するため1, 2)、食品中の微量の菌を迅速かつ高感度に検出・定量する方法の開発も求められている。
2.カンピロバクター属菌の新規定量的検出法カンピロバクター属菌の検出および定量には、国際標準化機構(ISO)の技術仕様書10272-1:2017および10272-2:2017 3,4)(以下、培養法)が広く用いられている。しかし、カンピロバクター属菌の培養には、次の①~④の特徴がある。 ①空気、乾燥、熱に極めて弱く、速やかに死滅すること ②実験的に長期間の培養又は大気中に暴露されると急速に菌形態をらせん状から球状に変化させ、速やかにVBNC(Viable But Non Culturable cells :生きているが人工培地で培養できない仮死状態)5,6)となること ③微好気環境で培養しなければならないこと7,8) ④遊走性をもつこと9) これらの特徴から人工培地を用いた菌数測定法では、感染、発症に至る実際の菌数を把握できない恐れがある。他方、MPN法(Most Probable Number:最確数法)は細菌数の少ない市販鶏肉の検査に用いられるが、時間と手間がかかり、検出範囲も狭い10)。そこで、代替法としてリアルタイムPCR法を用いた分子生物学的手法が開発された。リアルタイムPCRによる定量法(qPCR : quantitative PCR)は、CT値(PCR増幅産物がある一定量に達したときのサイクル数)を横軸に、初発のDNA量を縦軸にプロットし、検量線を作成し、そこから目的の検体中のDNA量を算出する方法である。qPCR法は培養法よりも感度が高く、低菌量の迅速な検出に用いることができる11)。しかし食品中の生菌数を測定する場合、qPCR法には、生菌と死菌を区別できないこと、食品成分によるPCR反応の阻害、DNA抽出のための特別な器具や技術が必要であることなどが課題とされている7)。したがって、食品中の成分の影響を受けにくく、死菌の影響を排除したqPCR法及びサンプリング法の開発が必要である。そこで筆者らはペーパーシートで食品を包んでサンプリングする「Wrap処理」(図1)を検討した。Wrap処理は従来法のように試料全体を潰すのではなく、試料を包んで表面にいる細菌を捕捉するサンプリング法である。そのため、食品成分や一次汚染微生物の影響が少ないことから、カンピロバクター属菌の増菌効率が高い。さらに増菌培養することで、死菌の影響を少なくし、高い検出精度で食品を汚染する微量のカンピロバクター属菌を定量できると考えた。 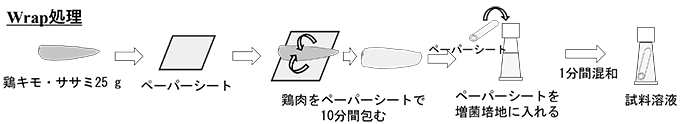 図1.Wrap処理のサンプリング法
Wrap処理でサンプリングした試料を増菌培養し、qPCRで増菌後の菌数を定量する手法の開発を試みた(図2)。qPCRは手順を簡略化し作業時間を短縮するために、試料液を直接PCRに供するDirect-qPCR法とした。Direct-qPCR法で検出したCT値から増菌前生菌数を推計するために、増菌培養前後の生菌数から回帰式(増菌回帰式)、そして、Direct-qPCR法で得られたCT値と増菌後生菌数から回帰式(PCR回帰式)が必要となる。そこで鶏キモと鶏ササミをカンピロバクター属菌標準菌で汚染し、これら2つの回帰式を作成し、CT値から推計した増菌前生菌数と、培養法で測定された生菌数を比較し、定量精度を検証した。
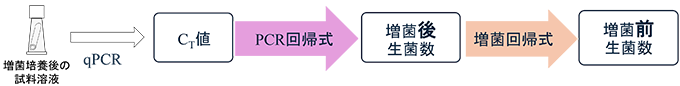 図2.Direct-qPCR法で検出したCT値から増菌前生菌数を推計する流れ
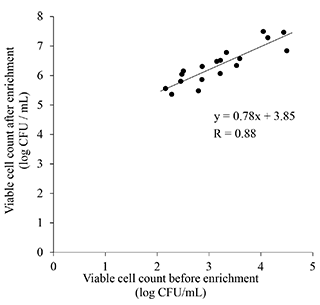
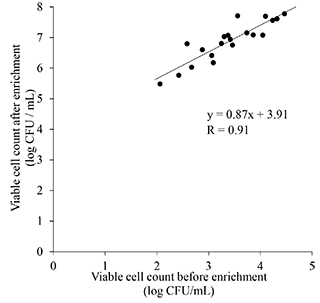
図3~6にカンピロバクター属菌標準菌で汚染したサンプルを用いた検証実験で得られた増菌回帰式及びPCR回帰式を示した。鶏キモ、鶏ササミともに相関係数の高い増菌回帰式、及びPCR回帰式が得られた。これら2つの回帰式を用いて図2の方法を検証したところ、推計した増菌前生菌数は培養法の生菌数より、鶏キモで0.72 log CFU低く、鶏ササミで1.10 log CFU低かった。推計した増菌前生菌数に、培養法の生菌数とDirect-qPCR法の推計値の比(推計値/生菌数)の平均値(キモ:1.27、ササミ:1.40)を係数として推計値に乗じたところ、生菌数と推計値に有意差は無かった12)。このことから、Wrap処理とDirect-qPCR法で測定すると、培養法と同等の値で増菌前菌数が1.0 log CFU/mL程度以上のサンプルで定量的検出が可能だと明らかになった。
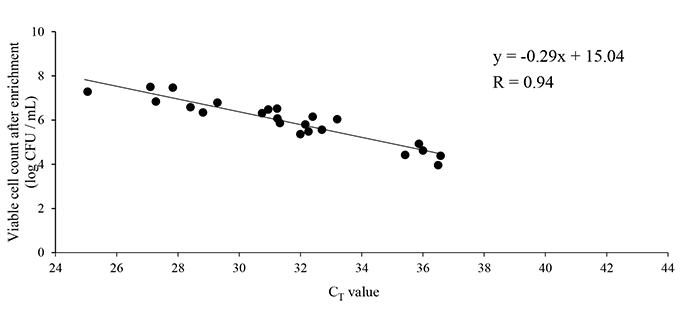 図5.PCR回帰式(鶏キモ)12)
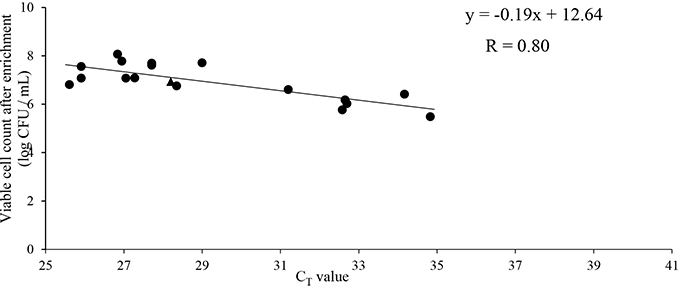 図6.PCR回帰式(鶏ササミ)12)
4.Direct-qPCR法を用いた定量的リスク評価前述のとおり、カンピロバクター食中毒予防対策を講じるためには、調理段階の汚染実態を定量する必要がある。そこで低菌量を定量的に測定できるDirect-qPCR法を用いて、三次汚染や除菌・殺菌効果を数値化するモデル調理実験を行った。 (1)三次汚染調理モデル実験 三次汚染調理モデルはカンピロバクター属菌の標準菌で汚染した鶏ササミを筋取りして二次汚染したまな板、包丁、手袋を用いて、生または茹でたほうれんそうを四つ切り、または、きゅうりを輪切り、千切り、乱切りにした。切った後の食材をDirect-qPCR法で生菌数を推計し、三次汚染率と汚染発生率(カンピロバクター属菌生残検出回数/実験回数×100)を求めた。 三次汚染調理モデルで三次汚染率を求めたところ、ほうれんそうを四つ切りする場合、茹での方が生より高率でカンピロバクター属菌が三次汚染した。汚染発生率は、まな板が92.9%(茹で)、100%(生)で高かった(表1)。きゅうりの場合、まな板から3.92~5.18%、包丁から0.80~1.69%、手袋から1.46~2.23%のカンピロバクター属菌が三次汚染した(表2)。三次汚染率を積算すると、一次汚染したカンピロバクター属菌の7.69%が茹でたほうれんそうに汚染し、4.51%が生のほうれんそうに汚染した(図7)。 ほうれんそうへの三次汚染率は、茹でが生より高値だった(表1、図7)。茹でることでほうれんそうの水分量が増え、二次汚染源との接触面積が増加するとともに、水の表面張力によりカンピロバクター標準菌が伝播しやすい条件だったと考えられる。 きゅうりでは輪切り及び乱切りより、千切りしたときに三次汚染率が高かった(表2、図7)。千切りはきゅうりとの接触面積が大きいことが要因と思われる。汚染発生率は、きゅうりを千切りしたとき包丁から45.5%、まな板からは100%だった(表2)。これは千切りしたとき、包丁ときゅうりの接触面積は小さいが、千切りした後のきゅうりはまな板と接触する面積が大きいことが影響したと考えられる。汚染発生率は三次汚染率と同様に接触面積や接触時間が大きいと高くなることが示唆された。
表1.三次汚染調理モデル実験結果(ほうれんそう)13)
表2.三次汚染調理モデル実験結果(きゅうり)13)
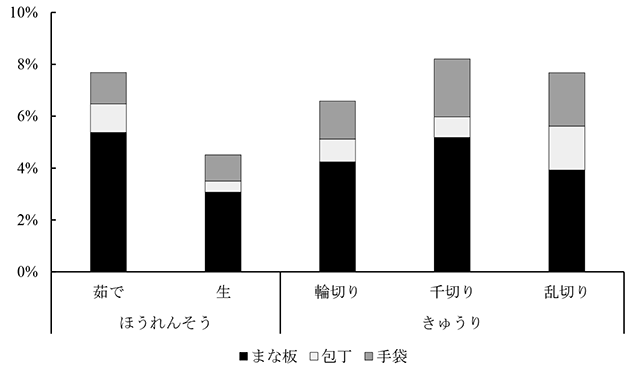 図7.三次汚染調理モデル実験結果(食材・切り方ごとの積算)13)
(2)除菌・殺菌モデル実験 除菌・殺菌モデルはカンピロバクター属菌の標準菌液(4~6 log CFU/mL)1mLをステンレス製トレーに滴下した後、以下のモデル操作を行った。 (a) 不織布ふきん(15×15cm)を直角に4つ折りして、面を変えて2回拭き取る (b) エタノール(76.9~81.4vol%)2mLを噴霧し1分間静置後、(a)と同様にふきんで拭き取る (c) 酸性電解水(有効塩素濃度30~40ppm)2mLを噴霧し1分間静置後、(a)と同様にふきんで拭き取る (d) ペーパータオル(21.8×23cm)を直角に4つ折りし、標準菌液を吸取後、エタノール2mLを噴霧し1分間静置後、(a)と同様にふきんで拭き取る (e) ペーパータオルを直角に4つ折りし、標準菌液を吸取後、酸性電解水2mLを噴霧し1分間静置後、(a)と同様にふきんで拭き取る 上記モデル操作後のトレーとふきんをDirect-qPCR法で生菌数を推計し、拭き取り後にトレーまたはふきんに生残したカンピロバクター属菌の割合(生残率)と生残発生率(カンピロバクター属菌生残検出回数/実験回数×100)を求めた。
表3.除菌・殺菌モデル実験結果(ふきん)13)
表4.除菌・殺菌モデル実験結果(トレー)13)
除菌・殺菌モデルにおいて、汚染菌液を拭き取ったふきんの生残率は最大2.94%と低率だったが、モデル操作による細菌の損傷や死滅、ふきんから検出される生菌数に定量上限があったことが原因と考えられた(表3)。汚染菌液を吸い取った後、殺菌剤を噴霧するとトレーにカンピロバクター属菌は生残していなかった(表4)。しかし、拭き取ったふきんにはカンピロバクター属菌が1.5 log CFU程度生残しており(表3)、ふきんが汚染源となるリスクがあること、ふきんの取り扱いに注意することを裏付けるデータが得られた。
5.終わりに「食品健康影響評価のためのリスクプロファイル~鶏肉等におけるCampylobacter jejuni/coli~(食品安全委員会)」で、消費者は「汚染鶏、鶏肉により容易に交差汚染が起こること、また調理段階において二次汚染が起こることに対する意識が低い」ことを指摘している。これは、これまで調理段階の汚染実態を定量したデータが少なかったため、消費者が二次汚染に関するリスクを正しく知る機会がなかったと考えられる。 Direct-qPCR法を活用した三次汚染調理モデル実験により、三次汚染率が最も高かったのはまな板であり、汚染発生率も高かった。鶏生肉などを扱う場合、まな板の洗浄・殺菌を行うことが重要であることが明確に示された。また、汚染源との接触面積が広いほど汚染率、汚染発生率ともに高いことを見える化した。また除菌・殺菌モデル実験により、トレーや調理台がドリップなどで汚染したときは、肉汁等をふきんで除去した後に、殺菌剤を噴霧することで、完全に調理台表面等からカンピロバクター属菌を除菌・殺菌できることが確認された。 調理段階の定量的リスク評価で必要なのは、同じ測定法でモデル実験を繰り返し行い、どの手順のリスクが高いのかを明確にすることである。Direct-qPCR法は24時間以内に結果が得られ、迅速・簡便にモデル実験を繰り返し行うことが可能で、定量的リスク評価に適した測定法であるとともに、食中毒の原因食品や伝播経路の調査にも適用できる。今後も調理モデル実験により、予防効果の高い方法やリスクの高い調理操作を把握し、情報提供に努めカンピロバクター食中毒予防対策の推進に役立ちたい。
参考文献
略歴
伊藤 智
神戸学院大学栄養学部 講師 神戸学院大学栄養学部 卒業、名古屋学芸大学大学院 栄養科学研究科 修了 博士(栄養科学)、管理栄養士 専門学校や大学の管理栄養士養成施設を経て、2015年4月から神戸学院大学 栄養学部 助教、2023年4月から現職。 食品衛生学や微生物学の講義・実験を担当。 日本栄養改善学会 評議員、日本防菌防黴学会 評議員を務めている。 国立循環器病研究センター主催 第6回 S-1g大会 医薬健栄研・災害栄養賞 金賞 令和5年度 日本防菌防黴学会誌 論文賞
サナテックメールマガジンへのご意見・ご感想を〈e-magazine@mac.or.jp〉までお寄せください。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Copyright (C) Food Analysis Technology Center SUNATEC. All Rights Reserved. |