|
グライセミックインデックス(GI)の有用性と問題点
新潟薬科大学 応用生命科学部 食品分析学研究室
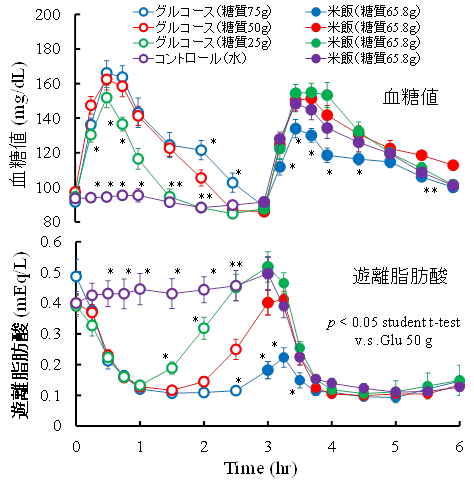
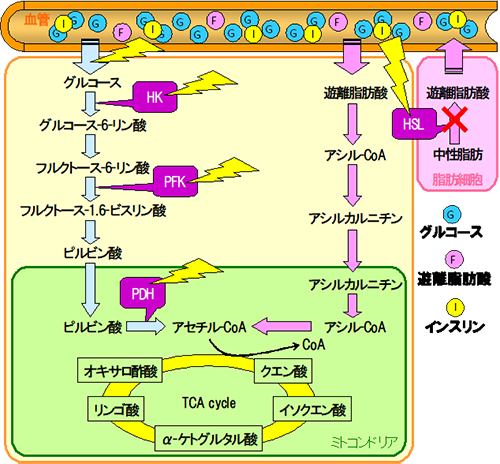
教授 佐藤 眞治 1. はじめにグライセミックインデックス(GI)とは、ブドウ糖50 gを摂取した後の血糖値‐時間曲線下面積(AUC)の値を100として、糖質50 gを含む食品を摂取した後のAUCより算出される。血糖値上昇が緩やかな低GI食品は、糖尿病性神経障害・網膜症・腎症などの合併症の発症予防に効果的であるが、高GI食品は、肥満症などの有病率と重症度を増加させることが報告されている。しかし、GIはその食品の固有な値ではなく、種々の要因によって大きく変動する。特に米飯のGIは、米穀の種類・調理方法・加工方法の違いによって、7~132と非常に大きくGIが変動するにも拘らず、高GI食品に分類されているのが現状である。本稿では、食物繊維・タンパク質・脂質などの食品成分の摂取によって、米飯(糖質食品)のGIが低下する可能性について述べる。更に、食品のGIの値はその食品を単独で与えた場合の値であるが、複数の食物繊維・タンパク質・脂質などの食品成分を同時に摂取させた場合や調理方法を組み合わせた場合、あるいはセカンドミール効果を利用することによってGIが大きく変動することについて述べ、「米飯のGIは不変な値ではなく、種々の要因によって大きく変動し、米飯の低GI化が可能である」ことの可能性について広く周知することを目的に、本稿を寄稿する。 2. グライセミックインデックスの有用性グライセミックインデックス(GI)は、食品摂取後の血糖値の上昇を客観的に表した数値と考えられている。ブドウ糖50 gを摂取した後の血糖値‐時間曲線下面積(AUC)の値を100として、糖質50 gを含む食品を摂取した後のAUCより算出される値であり、1981年にジェンキンスらが提唱した値である1)。GIに関する論文は非常に多く、PubMed を用いてGIを検索すると約1万件の文献がヒットする。日本においても2002年に日本Glycemic Index研究会が設立され、数多くのGIに関する研究成果が発表されている。日本Glycemic Index研究会は、「わが国において入手可能な食材、食品、食事について、Glycemic Index の観点からの研究の推進をはかり、その成果を広く啓蒙することにより、わが国における国民の健康増進に寄与すること」を目的として発足されている2)。このような啓蒙活動によって、日本国内の食品メーカーより低GI食品が多数販売されている。血糖値上昇が緩やかな低GI食品は、糖尿病性神経障害・網膜症・腎症などの合併症の発症予防に効果的であるが、高GI食品は、肥満症などの有病率と重症度を増加させることが報告されており3)、GIを用いた食事療法などが提案され、その有用性は実証されている。 3.グライセミックインデックスの問題点食品のGIは不変な値ではなく、種々の要因によって大きく変動する。その理由として、1)食事は単品ではなく、炭水化物や食物繊維以外にタンパク質や脂肪も含まれ、また調理方法も異なっているためにGI表どおりにはならないこと、2)摂食後の血糖値の変動が各個人で大きく異なる場合が多く、多数のボランティアを対象とするとGIのバラツキが大きくなること、3)ボランティアの耐糖能の状態が一定ではないためにGIが一致していないことなどが挙げられる。このようなGIのバラツキを大きくする要因は、GIの算出法にあると考えられる。GI算出法の最大の問題点は、食品摂取後の血糖値だけを用いてGIを算出している点にある。つまり、食品摂取後の血糖値の変動は、「消化管からの糖質の吸収速度」だけで決まるのではなく、「血中グルコースの消失速度:インスリンの分泌によって大きく変動する血中から組織中へのグルコースの取り込み速度」も密接に関与していると考えられる。従って、血糖値だけを用いてGIを算出した場合、同じGIであっても“消化管での糖質吸収の抑制によって得られたGIなのか”あるいは“膵臓からインスリンが過剰に分泌された結果として得られたGIなのか”を区別して評価することはできない。このことが同一食品でも同一のGIが得られない原因であり、また、GIのバラツキを大きくしている要因でもある。これらのことは容易に理解できるが、GIのバラツキを定量的に説明した報告は皆無であり、食品のGIの値だけが“独り歩き”しているのが現状である。その悪い例として、“低糖質ダイエット”が挙げられる。低GI食品は血糖値上昇が緩やかな食品であるため、単に食後の血糖値上昇を抑えるために極端に糖質の摂取を制限した“低糖質ダイエット”と混同され、非常に危険なダイエット情報の流布に繋がっている可能性がある。このような“低GI”と“低糖質”の混同は、食品のGIが固有な値であると思われているために生ずると考えられる。このような混同を払拭するためには、GIの理解が必要であり、「米飯のGIが固有の値ではなく、食物繊維・タンパク質・脂質などの食品成分の摂取によって低GI化する」可能性があるとの情報を広く周知させる必要があると考えられる。 4.米飯のグライセミックインデックス国民健康・栄養調査の結果によると、「肥満者(BMI ≧ 25 kg/m2)の割合は男性32.2 %、女性21.9 %であり、糖尿病が強く疑われる者の割合は男性18.7 %、女性9.3 %である」と報告されている4)。糖尿病、高血圧症、脂質異常症などのメタボリック症候群を予防するためには、内臓脂肪蓄積型の肥満症の発症を予防し、インスリン抵抗性の惹起を阻止することが非常に重要である。インスリン抵抗性を伴う糖尿病や糖尿病性合併症は、血糖値の上昇を十分にコントロールすることによってその発症を予防することが可能になる。即ち、摂食後の血糖値上昇の穏やかな食品を積極的に摂取することや抗酸化物質を積極的に摂取することにより、インスリン抵抗性を伴う病気の発症予防が可能になると考えられている。米飯は血糖値が上がり易い高GI食品であるため、メタボリック症候群の発症予防には適さない食品であり、肥満症を招く恐れのある食品とみなされている。米飯のGIは、白米が88、インディカ米が59、玄米が77、インディカ玄米が55など、デンプンの性質と食物繊維の含有率によって異なることが知られている5)。また、一般にデンプンは加水や加熱調理によって糊化し、アミラーゼなどの消化酵素の作用を受けやすくなり、血糖値が上昇し易くなる。糊化はアミロースとアミロペクチンの割合や混在する脂質やタンパク質などの他の栄養素の影響を受けることが知られている。実際、モチ摂取後の血糖AUCがグルコース摂取後の血糖AUCよりも大きく、モチのGIが100を超える場合がある6)。一方、米飯のGIは、米穀の種類・調理方法・加工方法の違いによって、7~132と非常に大きく変動することが報告されている7)。単糖類であるグルコースを多く含む食品や水分を多く含む食品を摂取すると、食物が素早く小腸へ移動するために血糖値が急激に上昇する。逆に、食物繊維・タンパク質・脂質を多く含む食品を摂取すると、インクレチンなどの消化管ホルモンの作用によって食物が胃に滞留するために血糖値の上昇が緩やかになる。このように、食品のGIの値はその食品を単独で与えた場合の値であるが、複数の食物繊維・タンパク質・脂質などの食品成分を同時に摂取させた場合や調理方法を組み合わせると食品のGIが大きく変動する。 5. 米飯の低GI化血糖値上昇が緩やかな低GI食品は、糖尿病性神経障害・網膜症・腎症などの合併症の発症予防に効果的であることは揺るぎのない事実であり、食事療法に積極的に取り入れるべきと考えられる。しかし、「米飯などは血糖値が上がり易い食品であるため、メタボリック症候群の発症予防には適さない食品であり、肥満症を招く恐れのある食品である」などの情報は払拭する必要があると考えられる。つまり、「食品のGIは不変な値ではなく、種々の要因によって大きく変動する」ことを実証し、広く周知させることが重要である。内臓脂肪量の増加は全身の糖代謝能を悪化させてインスリン抵抗性を惹起させる8)。運動療法や低GI食品を用いた食事療法など様々な手段によって内臓脂肪量の蓄積を減少させることは、糖代謝能を維持させるうえで重要であり、メタボリック症候群の発症予防に効果を発揮すると考えられている9)。食物繊維の摂取が多い群の肥満度は、食物繊維の摂取が少ない群に比べ有意に低くなることが報告されている3)。白パンを摂取した後の血糖値と血漿中インスリン濃度の上昇は、タンパク質を同時に摂取した場合に有意に抑制されることが報告されている10)。米飯を摂取する前にオリーブオイルなどの脂質をかけたサラダを米飯摂食すると血糖値や血漿中インスリン濃度の上昇が抑制されることが明らかにされている11)。更に、「セカンドミール効果」を利用して、米飯の低GI化が可能であると考えられる。「セカンドミール効果」とは、1回目の食事の内容が、2回目の食事の後の血糖値の上昇に影響を及ぼす効果であり、1988年にウォルヴァーらが指摘した効果である12)。図1に米飯のセカンドミール効果の例を示した。朝食に0、25、50、75 gのグルコースを健常成人に摂取してもらい、3時間後に昼食としてパック米飯1パック(糖質量65.8 g)を摂取してもらった。経時的に採血を行い、血糖値と血漿中遊離脂肪酸濃度の測定を行った。その結果、朝食摂取30分後の血糖値は約160 mg/dLに上昇し、3時間後には摂食前の値に戻ることが明らかになった。昼食摂取後の血糖値は、同じパック米飯を同量摂取しているにも関わらず、朝食にグルコースを75 g摂取した場合に、血糖値が有意に低く推移することが明らかとなった。前の食事の内容が次の食後の血糖値の変動に影響を及ぼすセカンドミール効果は、図2に示すランドルサイクルの考え方でうまく説明することができる。ランドルは、血液中のグルコースと遊離脂肪酸が密接に関連している回路(glucose-fatty acid cycle)が存在していることを提唱した13)。血液中の遊離脂肪酸は組織内に運ばれ、ミトコンドリア内でβ‐酸化をうけてアセチル‐CoAになる。このアセチル-CoAはピルビン酸に作用する酵素であるピルビン酸デヒドロゲナーゼ(PDH)やフルクトース‐6‐リン酸に作用するホスホフルクトキナーゼ(PFK)を阻害する。その結果、組織中のグルコース‐6‐リン酸が蓄積し、グルコースに作用する酵素であるヘキソキナーゼ(HK)が阻害されることによって血液中に存在するグルコースの取り込みが抑制され、インスリン抵抗性が惹起されるという仮説である。図1に示したように、朝食にグルコースを75 g摂取した場合、血漿中の遊離脂肪酸濃度はインスリンのホルモン感受性リパーゼ(HSL)の抑制作用によって、摂取後3時間においても他の投与量群に比べて低く推移している。これは、血液中のグルコースが組織中に取り込まれ易い状態であることを示している。実際、朝食にグルコースを75 g摂取させた場合、昼食後の血糖値の変動が他の摂取量群に比べ低く推移するセカンドミール効果が観察された。このように、米飯のGIは固有の値ではなく、食物繊維・タンパク質・脂質など食品成分の摂取やセカンドミール効果によって低GI化が可能であると考えられる。
図1. セカンドミール効果
図2.ランドルサイクル 6. おわりに「米飯のGIは不変な値ではなく、種々の要因によって大きく変動し、米飯の低GI化が可能である」ことを実証するためには、動物実験では限界があり、最終的にはヒトでの評価が必要である。しかし、ヒトを用いた試験を行う場合、倫理審査委員会を設置し、試験の倫理性及び試験方法の妥当性を審査し、「ヘルシンキ宣言」及び「人を対象とする医学系研究に関する倫理指針」に対応した試験実施体制を整える必要がある。更に多額の費用が発生する。「食物繊維・タンパク質・脂質などの食品成分の摂取によって米飯の低GI化が可能であった」との報告を期待したい。 参考文献
略歴
サナテックメールマガジンへのご意見・ご感想を〈e-magazine@mac.or.jp〉までお寄せください。 |
| Copyright (C) Food Analysis Technology Center SUNATEC. All Rights Reserved. |