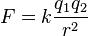| ◆ HOME > 食品製造加工機器表面への汚れの付着機構 |
 |

食品製造加工機器表面への汚れの付着機構
 東京海洋大学 食品生産科学部門
教授 萩原 知明
1.はじめに
食品製造装置や食品調理器具・設備に付着残存した汚れは食中毒菌や腐敗菌などの微生物にとっての格好の生育の場となる。従って、食中毒汚染ならびに食品品質劣化のリスクを軽減し、製品の安全性を確保しかつ品質劣化を抑制するためには、洗浄は必要不可欠である。一方で、洗浄は、多量の水とエネルギーを必要とするが、地球環境保全の観点から、限りある水資源を有効に使用することが世界的に求められており、洗浄に使用する水、薬品ならびにエネルギーの削減が待ったなしの状況にある。このような状況に的確に対処するためには、洗浄に関わる諸現象を科学的に理解し、合理的な指針に基づき、適切な洗浄条件を構築する他ない。しかしながら、洗浄に関する科学的な検討は遅れているといわざるを得ない。洗浄は我々にとって身近かつ重要な存在であるにも関わらず製造工程の後始末という感覚が長年あったことがその一因であろう。また、洗浄は食品の安全性と密接に関わる極めて重要な操作であるがために、「今まで上手くいっている(注;実は顕在化してないだけで、問題や課題がある場合が少なくない)方法を、なぜ変える必要があるのか?」「新しいやり方に変えて、問題が起きたらどうするのか?」といった考えから、洗浄方法は「保守的」になりがちである。その結果、新規の手法や考え方の導入が遅れ、経験がものをいう世界になっている側面もあろう。近代科学の理念の一つに、Evidence-based(エビデンスベイスト)がある。実験データや実例など具体的かつ合理的な根拠(Evidence)に基づいて理論や手法を構築することを指す。例えば、Evidence-based medicine(根拠に基づく医療)のような使われ方をする。振り返ってみるに、上記の現在の洗浄課題解決のために必要なのは、根拠の薄い経験や試行錯誤よりもEvidence-based cleaning(EBC;根拠に基づく洗浄)ではないだろうか?優れた新規洗浄方法の開発を望む人は多いだろうが、その革新技術を使いこなすためには技術の原理原則の理解が必要である。また、既存の洗浄技術であっても原理原則の理解の基に用いることでより効果的かつ効率的な洗浄の実現が可能となるはずである。
以降、本報では洗浄の効率化、体系化を考える上で、重要となる汚れの付着機構に関して述べる。汚れの付着・蓄積のメカニズムを知ることは、付着・蓄積の抑制方法を考える上で重要な知見であり、効率的な洗浄の実現へと繋がる。
2.汚れの付着に係る相互作用[1]
一般に、汚れは自然発生的に生じる。遊離状態の物質が何らかの相互作用を介して表面に吸着し「汚れ」となる。「自然発生的」とは、物理化学的には自由エネルギー変化(ΔG)が負の現象であることを意味している。つまり、汚れを脱離させるためには外部から付着エネルギー以上のエネルギーを費やさなければならない。
汚れの付着をもたらす代表的な相互作用は、以下の4つである。
①静電的(クーロン)相互作用
②ファンデルワールス(van der Waals)相互作用
③疎水的相互作用
④水素結合
以下、それぞれを詳細に説明する。
①静電的(クーロン)相互作用
電子を放出または受け取って電荷を帯びた原子または原子団(分子)をイオンとよぶ。陽イオン同士、陰イオン同士には反発しあう力が働き、陽イオンと陰イオンには引力が働く。rの距離で離れている2つの電荷q1、q2の間には、以下の式で表される力Fが作用する。この場合マイナスの力は引力、プラスの力は斥力(反発)を意味する。
②ファンデルワールス(van der Waals)相互作用
イオンのように恒常的に電荷を帯びていない分子間にも力が働く。例えば、窒素やアルゴンはイオンではないが、温度を十分下げると気体から液体に変化する。これは分子間に引力が働いている証拠である。このような分子間に働く力をファンデルワールス力という。ファンデルワールス力の発生するメカニズムの説明は少々難解であるが、説明をしておく。イオンのように電荷を帯びてない分子であっても、分子内の原子や結合の違いによる電荷の偏りが存在する場合があり、引力が働く。また、定常的に電荷の偏りが存在していない分子であっても、現実には電子が運動しているため、瞬間、瞬間には電気的な偏りを生じ、この偏りによりクーロン力が誘起されて引力が働く。これらを総称して、ファンデルワールス力とよぶ。このうち、後者の電子の揺らぎにより誘起されるものを分散力とよぶ。分散力は、イオンを含むあらゆる種類の分子間に普遍的に作用する力である。
③疎水的相互作用
「疎水性」とは、水に対する親和性が低い性質のことである。疎水性物質は一般に、電気的に中性の非極性物質である。「疎水性」の対義語は「親水性」である。一般的に極性の高いまたは電荷を有する化合物は親水性を示す。
疎水性の物質が水中に存在しているとき、疎水性分子は水にはじかれ、互いに凝集集合する。これを疎水効果とよぶ。疎水的相互作用は、疎水効果によって非極性分子間に働く引力的相互作用をあらわし、疎水性分子同士に固有の引力が働いて生じるのではなく、水からの逃散の結果生じることに注意されたい。
④水素結合
水素結合は、電気陰性度が大きな原子に共有結合で結合した水素原子が存在している系で生じる。電気陰性度が大きい原子は、電子を引き付ける作用が大きいため、水素原子は正電荷を帯びる。このとき、水素原子近傍に窒素、酸素、硫黄、フッ素などの陰性原子が存在すると、静電的作用により引力が生じる。ただし、通常の静電的相互作用のような方向性のない相互作用ではなく、水素原子と陰性原子の相対的な配置にも依存する相互作用である。
実際の汚れの付着は、これらの複数の相互作用が関与して起こる。例えば、酸性条件下でのβ-ラクトグロブリン(乳清の主要なタンパク質。乳由来のアレルゲンでもある)のステンレス鋼表面への付着は、ファンデルワールス相互作用を介して初期付着が起こり、次にβ-ラクトグロブリンに存在する解離した酸性アミノ酸残基由来の負電荷と、ステンレス鋼表面の正電荷の間の静電的引力により付着がより強固なものになると提唱されている[2]。
3.汚れの付着挙動の例
タンパク質の付着
タンパク質は難洗浄性の汚れを形成することが知られており、食品製造機器の洗浄の主要なターゲットとなっている。食品機械装置の素材として一般的に用いられているステンレス鋼との付着挙動に関する研究がこれまで数多くなされてきている。
タンパク質はファンデルワールス力や水素結合の疎水的相互作用ならびに静電的相互作用などの複数の相互作用を通じて、ステンレス鋼表面に付着する。ステンレス鋼表面に直接吸着したタンパク質は、洗剤を含まない水による洗浄ではほとんど落ちない。例えば、ホッコクアカエビ(通称名アマエビ)の身から水抽出したタンパク質をステンレス鋼に付着させた後、蒸留水で洗浄を行っても、明確な付着量の減少は見られなかった[3]。これは、エビ・カニ等の甲殻類の主要なアレルゲンとして知られているトロポミオシンも同様であった[3]。興味深いのは、塩濃度が低い条件下では、トロポミオシンは他のタンパク質と比較して、ステンレス鋼表面に極めて付着しやすいことである[3]。このことは、トロポミオシンはステンレス鋼表面に汚れとして付着残存しやすいことを意味している。
pHやイオン強度が変化すると、固体表面ならびにタンパク質の電気的性質が変化し得るので、付着量は影響を受ける[4]。 また、筋肉組織を含む食品においては、イオン強度が増加すると、筋原線維タンパク質が可溶化するため、付着し得るタンパク質の種類が異なる事態が生じ、付着量や付着挙動が影響を受けることがある[5]。
付着したタンパク質分子はそのままの状態で留まるのではなく、固体表面との相互作用による変性や、付着したタンパク質間の相互作用を通じた緻密化等の過程を経て、汚れ層が形成されていく[4, 6]。このような過程を通じて、タンパク質と固体表面との結合が強固となっていくと考えられる。
一般に、タンパク質付着量はタンパク質の変性温度より低温では、タンパク質分子が固体表面を一層覆ったところで汚れの蓄積は止まる。変性温度以上では、タンパク質分子間に加熱凝集反応が起こることで、さらに汚れの蓄積が進む[4, 7-9]。このことは、タンパク質を多く含む食品由来汚れに対しては、高温での洗浄が洗浄効果の低下を招く可能性があることを意味している。まず、予備洗浄として、タンパク質の変性温度以下の水による洗浄を行い、固体表面に緩く付着している汚れまたは隙間や配管内に詰まっている汚れを除去することで、これらの汚れが加熱凝集反応で固体表面に付着しないようにする必要がある。
微生物(細菌)の付着
微生物が他の汚れと異なる点は、環境の条件に応じて増殖し得ることである。微生物の付着汚れの形成は以下の段階を経て進行する[10]。
- 第1段階:
- 固体表面へのイオン、有機物の吸着によるコンディショニング・フィルム(Conditioning film)の形成
- 第2段階:
- コンディショニング・フィルム への微生物の付着
- 第3段階:
- 微生物および細胞外多糖(Extracellular polysaccharide;EPS)からなるバイオフィルムの成長
- 第4段階:
- 微生物密度の過密化にともなうバイオフィルムの崩壊と微生物の外部への放出
第1段階においてコンディショニング・フィルムが形成されることにより、微生物の付着が促進される。洗浄不足で残存した汚れは、コンディショニング・フィルムとして作用することになる。第2段階までの微生物は付着と脱離を繰り返しており、付着した微生物の除去は比較的容易である。しかしながら、第3、4段階へと進むと、微生物は表面に強く付着し、その除去のための手間は増大する。第3、4段階において、微生物は自ら生産したEPSの中に埋め込まれたような形態で存在している。EPSと微生物から形成されている構造体をバイオフィルムとよぶ。EPSは物質運搬経路ならびに微生物保護の役割を果たしており、外部環境変化(温度、物質濃度変化等)から内部の微生物を守る。その結果、バイオフィルム内には、菌体が高密度で生育し、恒常性が保たれる。
バイオフィルム中の微生物は、遊離状態の微生物と比較して、熱や薬剤に対する抵抗性を示す。例えば、バイオフィルム中のListeria monocytogenes(リステリア菌)は、遊離菌が検出限界以下まで死滅する70℃、5分の加熱後も生き残った[11]。また、遊離菌が30秒の処理で検出限界以下になる薬剤処理に対しても、20分処理後も生き残った[11]。これらの耐性は、EPSの存在により、伝熱や薬剤の浸透が妨げられるためであると考えられている。
食品製造機器や食品の主要な殺菌対象となる芽胞菌は、栄養細胞と比較して、熱、薬剤、乾燥に対する耐性が強く、万が一、固体表面に付着残存した場合、衛生上のリスクは、栄養細胞よりも持続することになる。そのため、芽胞菌の付着挙動に関する情報は重要である。ステンレス鋼およびポリプロピレン表面に付着させた芽胞菌(Geobacillus stearothemophilusおよびBacillus subtilis)は、湿潤状態では水洗浄で除去できるが、乾燥すると水洗浄および0.2%水酸化ナトリウム洗浄では落ちない[12]。このような強固な付着が生じる機構は明らかにはなっていないが、菌体と固体表面との間の疎水的相互作用の関与が示唆されている[12] 。
4.おわりに
以上、汚れの付着に関する相互作用ならびに汚れの付着挙動の例として、タンパク質および微生物の付着について述べた。食品および微生物の種類の数だけ汚れの種類は存在し、また温度、pH、塩濃度などの外的条件、固体表面の種類に応じて付着挙動は変化する。汚れの付着に関しては、まだまだ分からないことだらけである。本報を通じて、より多くの方が、洗浄に関する研究に興味を持って頂ければ幸いである。
参考資料
- 1.
- 久保田清, 村田博, 中西一弘 「食品工学基礎講座:輸送と洗浄」, 光琳, 1989.
- 2.
- T. Hagiwara, T. Sakiyama, H. Watanabe, Molecular simulation of bovine b-lactoglobulin adsorbed onto a model positively charged solid surface. Langmuir 5: 226-234(2009).
- 3.
- S. Thammathongchat, T. Hagiwara, T. Sakiyama, Adsorption of tropomyosin from pink shrimp(Pandalus eous)on stainless steel surface. Food Control 21: 1250-1253(2010).
- 4.
- K. Nakanihi, T.Sakiyama, K. Imamura, On the adsorption of proteins on solid surfaces, a common but very complicated phenomenon. Journal of Bioscience and Bioengineering 91: 233-244(2001).
- 5.
- S. Ratanasumawong, T. Hagiwara, T. Sakiyama, Effect of sodium chloride on adsorption of shrimp proteins from pink shrimp(Pandalus eous)on stainless steel surface. Food Science and Technology Research 21: 327-331(2015).
- 6.
- T. Hagiwara, P. Nattawut, M. Shibata, T. Sakiyama,Monitoring of adsorption behaviors of bovine serum albumin onto a stainless steel surface by the quartz crystal microbalance based on admittance analysis. Bioscience Biotechnology and Biochemistry 81: 783-789(2017).
- 7.
- H. Ito, A. Nagata, T. Toyomasu, T. Sakiyama, T. Nagai, T. Saeki, K. Nakanishi,Adsorption of β-lactoglobulin onto the surface of stainless steel particles. Bioscience, Biotechnology, and Biochemistry 59: 1648-1651(1995).
- 8.
- T. Hagiwara, M. Suzuki, Y. Hasegawa, S. Isago, H. Watanabe, T. Sakiyama, Temperature effect on pink shrimp(Pandalus eous)protein adsorption onto a stainless steel surface. Food Science and Technology Research 21: 341-345(2015).
- 9.
- T. Hagiwara, S. Hagihara, A. Handa, N. Sasagawa, R. Kawashima, T. Sakiyama, Pretreatment with citric acid or a mixture of nitric acid and citric acid to suppress egg white protein deposit formation on stainless steel surfaces and to ease its removal during cleaning. Food Control 53: 35-40(2015).
- 10.
- 日本微生物生態学会バイオフィルム研究部会編著 「バイオ フィルム入門」 日科技連出版社, 2005.
- 11.
- J. F. Frank, R. A. Koffi, Surface-adherent rowth of Listeria monocytogenes is associated with increased resistance to surfactant sanitizers and heat. Journal of Food Protection 53: 550-554(1990).
- 12.
- Y.Nanasaki, T.Hagiwara, H.Watanabe, T.Sakiyama, Removability of bacterial spores made adherent to solid surfaces from suspension with and without drying. Food Control 21: 1472-1477(2010).
略歴
- 平成4年3月
- 東京大学農学部農芸化学科 卒業
- 平成4年4月
- 東京大学大学院農学研究科農芸化学専攻修士課程 入学
- 平成6年3月
- 同 修了
- 平成6年4月
- 東京大学大学院農学生命科学研究科応用生命化学専攻博士課程 入学
- 平成9年3月
- 同 修了
- 平成9年4月
- 東京水産大学水産学部 助手
- 平成22年10月
- 国立大学法人 東京海洋大学海洋科学部 准教授
- 平成27年6月
- 国立大学法人 東京海洋大学海洋科学部 教授
- 平成29年4月
- 国立大学法人 東京海洋大学海洋生命科学部 教授 現在に至る。
|