| ◆ HOME > 食品製造機器の洗浄性を評価するための試験方法の提案 |
 |

食品製造機器の洗浄性を評価するための試験方法の提案
 三重大学大学院生物資源学研究科
教授 福崎 智司
はじめに
近年、食品製造現場では設備や機器(機械、装置、器具)の清浄度を維持するための洗浄・殺菌操作の効率化が課題となっている。特に、製品が直接接触する機器表面の清浄度は、製品の二次汚染と密接に関係しており、高い清浄度が求められている。機器の洗浄性は、構造、構成、材質、設置等を考慮した衛生構造の影響を強く受ける。食品加工機械の安全・衛生に関する設計要求を定めたJISでは、衛生構造に対する要求事項は、具体的な数値を定めない性能要求にとどまっている1)。また、日本では食品加工機械の洗浄性を自主検証する試験法は定められていない。その理由の一つとして、機械表面に塗布する標準的な試験用汚れの設定が困難であることが挙げられる。また、洗浄後の残留汚れ量を定量的に評価する方法を定める必要がある。
従来、定置洗浄性を評価する方法として、EHEDG(欧州衛生工学設計グループ)が提示する試験方法が存在する2)。この試験方法では、汚れとして酸敗牛乳(酸乳)と好熱性芽胞形成菌の混合物を用いる。洗浄には中性(~弱アルカリ性)洗剤を使用し、洗浄後の清浄度の評価には残留した芽胞菌の増殖過程で生成する酸を培地中の呈色試薬で検出し、色見本を用いて目視判定する。このとき、比較対照となる基準パイプにある程度の汚れが残るように調整する。この試験方法の課題として、各現場での酸乳の調製が均一でない、操作が煩雑である、清浄度の評価が定量的でない、機器の構造にかかわらず洗浄によって汚れが完全に除去される等が挙げられ、試験用汚れの調製にも課題が残されていた。
筆者らは、定置洗浄性試験の簡易化を目的として、試験用汚れの調製と拭き取り法による表面汚れの定量評価法の確立に取り組んでいる。試験用のモデル汚れに望まれる特性としては、①食品成分であること、②安価に入手可能な成分で構成されること、③調製が容易であること、④汎用的な分析機器で定量できること、⑤衛生構造の不良や洗浄力不足が残存量として明確に反映されること、⑥洗浄における汚れの構成成分の離脱挙動に相関性があることが挙げられる。この点において、乳タンパク質は固体表面に対する吸着親和性が高く、様々な食品成分と多様な相互作用を示すことから、モデル汚れの主成分として適している。
本稿では、ステンレス鋼表面に残留した種々のタンパク質、細菌の定量評価のための拭き取り操作の標準化と、乳タンパク質を汚れの主成分とする簡易試験用汚れの調製について紹介する。また、蛍光色素と蛍光検出法を用いた非接触方式での表面清浄度の評価についても触れてみたい。
1.拭き取り操作の標準化3)
1.1 タンパク質の定量法とスワブ棒の選定
拭き取り操作の標準化の第一段階は、汚れの指標とするタンパク質の定量法を決めることである。一般的に、タンパク質の定量には、発色試薬(比色法)の利用が有効である。筆者らは、定量範囲が上限・下限とも広く再現性の高いLowry-Folin 法4)を採用している。
拭き取り量の検出では、スワブ棒も反応試薬中に浸漬するため、反応試薬に対して不活性な(呈色しない)材質のスワブ棒を選定する必要がある。ここで、従来からスワブ棒として汎用されている綿棒には、Lowry-Folin法に用いる試薬(フェノール試薬+ビウレット反応試薬)との反応性に短所がある。
表1に、先端部と軸部の材質が各々異なる市販のスワブ棒を用いて、Lowry-Folin法に用いる試薬との反応性(吸光度:Abs750)を比較した結果を示す。実験に供したスワブ棒([先端]/[軸])は、以下の3種類である。
①ポリエチレン(PE) /ポリプロピレン(PP)
②綿/紙
③綿+レーヨン(CR)/紙
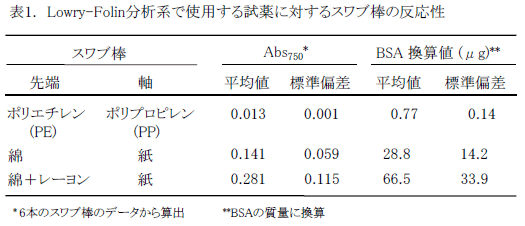
スワブ棒自体の反応性は、拭き取り操作後のタンパク質定量系のブランク値に相当する。PE/PPスワブ棒の反応性は、Abs750で0.013ときわめて小さく、標準偏差(SD)も0.001とばらつきの小さい材質であることがわかる。この値は、ウシ血清アルブミン(BSA)相当量に換算して0.77μg (SD=0.14)であり、ブランク値として定量系に影響を与えない数値である。一方、綿/紙スワブ棒およびCR/紙スワブ棒の反応性は、BSA換算量で各々28.8 μg(SD=14.2)および66.5 μg(SD=33.9)であり、比較的大きい反応性とばらつきをもつ材質であることがわかる。スワブ棒のブランク値とそのばらつきが大きい場合、50 μg程度以下の微量の付着BSAを精度良く検出することは望めない。このように、Lowry-Folin定量系では、PE/PPスワブ棒のような不活性な材質を用いる必要がある。
筆者らが選定したPE/PPスワブ棒は、PE先端部が筆ペン様の柔軟性・復元性に富む構造で、適度な吸水性(飽和吸水量:70μl)がある。拭き取り操作は、スワブ棒の先端部をタンパク質付着ステンレス鋼板に対して約45°の角度を保ちながら手動により約20秒間往復させて拭き取ることを基本としている(下記参照)。
1.2 拭き取り操作
(1)湿潤液
PE/PPスワブ棒先端部の湿潤液は、ステンレス鋼表面からスワブ棒にタンパク質を移行させるための媒体として不可欠である。
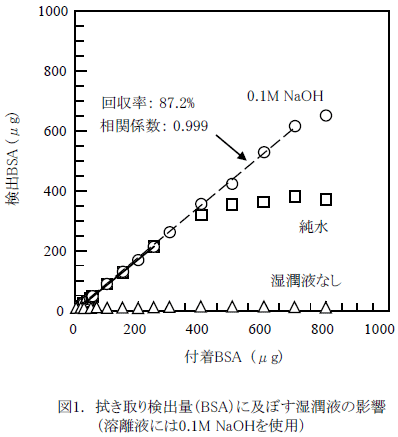
図1に、ステンレス鋼板に付着させたBSA(40℃で乾燥)を対象に、湿潤液として①純水(イオン交換水)、②0.1M NaOH水溶液を用いた場合と、③湿潤液なしでの拭き取り操作を行ったときの結果を示す(溶離液には0.1M NaOHを使用)。付着量が250 μg以下の場合、純水およびNaOH水溶液とも回収率はいずれも87%、相関係数は0.999の結果が得られている。重要な点は、回収率よりも、良好な直線関係(再現精度)が得られるか否かである。NaOH水溶液を用いたときの利点は、直線性が得られる付着量の範囲が広がる(~700 μg)点である。ただし、湿潤液が拭き取り面に残ると回収率は低下することから、PE先端部へは飽和吸水量の85%程度(この場合は60 μl)に湿潤液を吸水させることが望ましい。
一方、湿潤液を用いない場合(乾拭き)、タンパク質検出量は<8 μgとなり、ほとんどタンパク質を拭き取ることはできない。
(2)スワブ棒の押しつけ力
拭き取り操作を上皿天秤の上で行うことにより、押しつけ力(Fp)と回収率の関係を調べることができる。PE/PPスワブ棒と0.1M NaOH水溶液を用いた拭き取り系では意外に強い力は必要なく、80~140 gfの力で擦りつけるように往復させて拭き取ることにより高い回収率が得られる。このFpの範囲以下では力が不足し、範囲以上では過剰となるが、たとえ過剰なFpでも回収率が低下するわけではない。
一方、タンパク質は熱による変性を受けると高次構造が変化して疎水化や凝集が起こり、水への溶解度が低下する。そのため、実際の現場では、付着後の熱変性タンパク質の場合は、Fpを高める必要がある。検討の結果、100~150℃で熱変性したBSAに対しては、Fpを200gf程度に高めると95%以上の高い回収率が維持できることを確認している(結果未掲載)。
(3)溶離液
疎水性のポリマー表面は水に対する濡れ性が低いことから、NaOH水溶液の洗浄作用(溶離作用)を受けにくい性質を持つ。PE先端部もNaOH水溶液に濡れにくい性質であることから、溶離効率を高めるためにはPEとNaOH水溶液の界面張力を低下させる必要がある。0.1M NaOH水溶液にドデシル硫酸ナトリウム(SDS)を0.1% (w/v)添加することによって、Lowry-Folin法による検出を妨害することなく、PE先端部からのタンパク質の溶出効率を高めることができる。溶離時間は、少なくとも5分間で十分である。SDSの使用により、図1で得られた回収率(87%)は97%まで増加する。
(4)標準操作条件
硬質表面にステンレス鋼、タンパク質にBSA、タンパク質定量法にLowry-Folin法を用いた検討の結果、導かれた拭き取り操作の標準的な手順および設定条件は以下の通りである。
①スワブ棒:PE/PPスワブ棒
②湿潤液:0.1M NaOH水溶液(平衡吸水量の85%相当)
③スワブ棒押しつけ力:約200 gf(熱変性していなければ80~140 gfでも可)
④スワブ棒の角度:45°(任意)
⑤拭き取り時間:20秒(50×50 mmの面積の場合)
⑥溶離液:0.1% (w/v)SDSを含有する0.1M NaOH水溶液
⑦溶離時間:5分
1.3 拭き取り操作条件の検証事例
上記の標準操作条件に従って、卵アルブミン(EA)および大腸菌(E. coli)を付着させたステンレス鋼(40℃で乾燥)を対象に拭き取り操作の妥当性を確認している。
図2は、EAの付着量1~720 μgの範囲における付着量とスワブ法による検出量の関係である。図中の実線は、線形最小二乗法によるデータ適合の結果である(相関係数0.999)。グラフの傾きから、平均の回収率は97.7%と算出された。
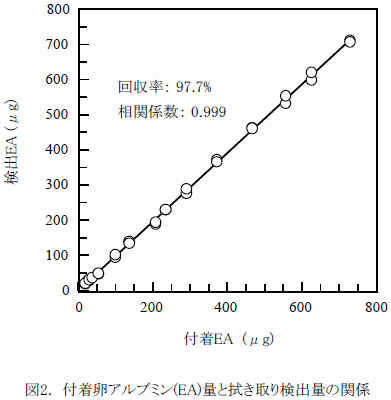
この実験系における付着量1 μgは、単位面積あたりの付着量に換算すると約3.2 mg/m2に相当する。これは、タンパク質分子の単分子層吸着と同桁の値である。このように、実際の機器に付着・残留しやすいEAに対して、適切な拭き取り操作を行えば単分子層吸着のレベルまで検出可能である。ちなみに、湿潤液を使用しなければ、付着EA(1~720 μg)はほとんど回収できない。
図3に、E. coliの付着菌体数(CFU)とスワブ法による検出菌数の関係を示す5)。この実験では、拭き取り回収した菌体のタンパク質定量値から菌体数を概算している。付着菌体数0.1~4.1×108 CFUの範囲で、良好な直線関係が得られている。線形最小二乗法による解析の結果、回収率は96.5%、相関係数は0.999と算出された。これは、タンパク質を対象とした拭き取り操作で得られた拭き取り精度と同等の値であった。
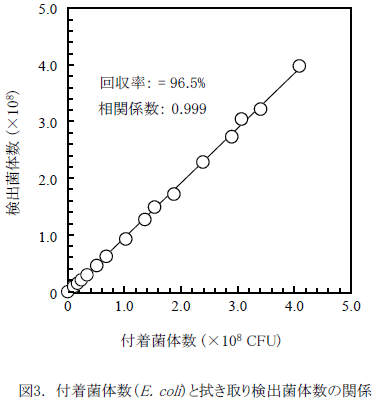
以上の結果から、BSAの拭き取りを対象に提案されたPE/PPスワブ棒を用いた標準拭き取り操作条件に従えば、ステンレス鋼板に付着した他のタンパク質や細菌菌数を精度良く測定できることがわかる。
2.簡易試験用汚れの調製6)
洗浄における汚れの離脱性は、媒体である水への溶解度と密接に関係している。乳タンパク質の場合、溶解度の低下を誘発する要因として、タンニンなどのポリフェノールとの結合による難溶性物質への変化7, 8)や、加熱処理による熱変性と凝集が挙げられる9)。この2つの要因は、汚れの固着度を制御するうえで好適な現象といえる。
2.1 試験用汚れ構成成分と調製法
モデル汚れを構成する物質として選定したのは、低脂肪加工乳(市販品)と0.5%タンニン酸水溶液、2.5% β-ラクトグロブリン水溶液と0.5%タンニン酸水溶液、2.5%カゼインナトリウム水溶液と0.5%タンニン酸水溶液の等量混合物である。また、0.2%クルクミンエタノール溶液(95%エタノールにクルクミンを溶解)を添加したカゼインナトリウム/タンニン酸混合水溶液を用いて、色素を指標として清浄度を定量化する系も検討している。
各モデル汚れ原液10 μlをステンレス鋼板(SUS 304; 50×50×1 mm)の表面上に滴下し、直径約20 mmとなるように塗り広げる。汚れを塗布したステンレス鋼板を40℃の乾燥器内で16時間乾燥して汚れ付着ステンレス鋼とする。さらに、汚れの固着度を制御するために、上述のステンレス鋼板を再度40~140℃の乾燥器内で2時間加熱処理する。
2.2 洗浄方法
洗浄液として、水洗浄にはイオン交換水(pH 6)、アルカリ洗浄には0.1M NaOH水溶液(pH 13)を用いる。汚れ付着ステンレス鋼板を25℃に保温した各洗浄液150 ml中に2時間浸漬し、イオン交換水中ですすぎを行った後、ステンレス鋼板を40℃で24時間乾燥して清浄度の評価に供する。
2.3 加熱温度と汚れの残存率
(1)低脂肪加工乳とタンニン酸の混合物
図4に、低脂肪加工乳とタンニン酸の混合物を付着させたステンレス鋼板を種々の温度で加熱処理した後、水洗浄およびアルカリ洗浄を行ったときの加熱温度と汚れの残存率の関係を示す。水洗浄の場合、汚れの残存率は、加熱温度が40~80℃の範囲では約5~18%であったが、100℃で68%、さらに120℃以上では89~95%まで著しく増加している。アルカリ洗浄の場合、汚れの残存率は40~120℃範囲では2%以下であるが、130~140℃では39~44%に増加する。
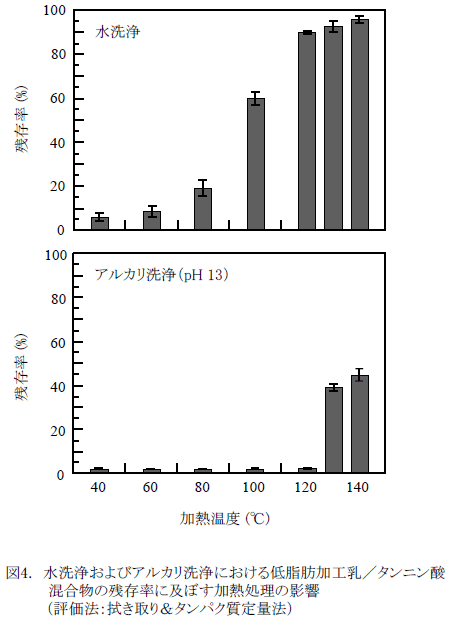
低脂肪加工乳の加熱処理の場合、80℃以上でホエータンパク質の熱変性に起因する不溶化とS-S結合を介する凝集が起こる。この不溶化と凝集は、タンニン酸の存在によって促進され、ステンレス鋼表面への固着度は増加する。
一方、125℃以上での加熱(2時間)では、カゼインの熱変性が起こるため10)、汚れの不溶化は一層促進されることになり、アルカリ洗浄(OH-の洗浄作用)では十分に除去できない固着汚れに変化したと考えられる。
低脂肪加工乳は入手しやすいタンパク質系汚れの原料となり得ることがわかったが、原料の生乳に依存した低脂肪加工乳の成分変動を考慮すると、さらに単純化した組成で汚れを構成することが望ましい。そこで、乳タンパク質の成分としてホエータンパク質であるβ-ラクトグロブリンと水可溶性のカゼインナトリウムの利用を試みた。
(2)β-ラクトグロブリンとタンニン酸の混合物
図5に、β-ラクトグロブリンとタンニン酸の混合物を汚れとして用いた時の、水洗浄後およびアルカリ洗浄後の汚れの残存率の関係を示す。水洗浄の場合、汚れの残存率は、加熱温度に依存して徐々に増加する傾向を示しており、β-ラクトグロブリンの熱変性と一致する挙動を示している。140℃では、残存率は100%となり、水洗浄ではまったく除去できない汚れに変化する。
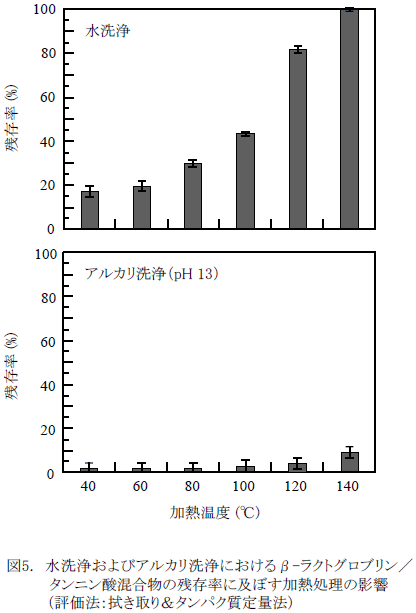
一方、アルカリ洗浄における残存率は一様に低く、140℃においても10%以下となるなどアルカリ洗浄単独でも比較的容易に除去できる汚れであることがわかる。低脂肪加工乳とタンニン酸の混合物の結果(図4)と比較すると、130~140℃における高い残存率はβ-ラクトグロブリンの熱変性に起因するものではないことを示している。
(3)カゼインナトリウムとタンニン酸の混合物
図6に、カゼインナトリウムとタンニン酸の混合物を汚れとして用いた時の、水洗浄後およびアルカリ洗浄後の汚れの残存率の関係を示す。水洗浄の場合、汚れの残存率は80~100℃の間で顕著に増加している。一般に、カゼインは100℃以下での加熱には安定であることから、タンニン酸との結合によりカゼインの熱安定性が減少して不溶化したのではないかと考えられる。アルカリ洗浄の場合、汚れの残存率は40~100℃範囲では3%程度であったが、130~140℃では30~35%に増加する。
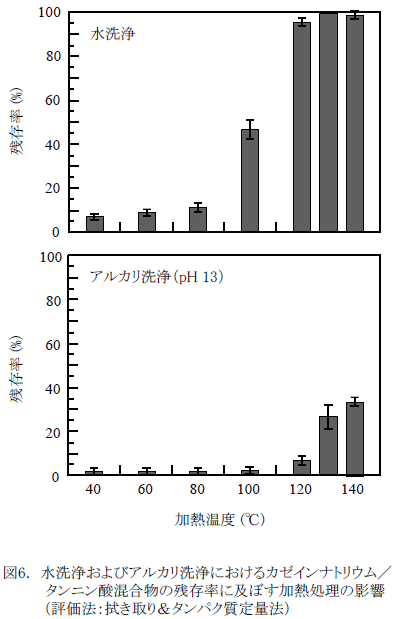
以上の加熱温度と残存率の関係は、低脂肪加工乳とタンニン酸の混合物の結果にきわめて類似していることから、カゼイン/タンニン酸結合体の加熱物の固着性が乳タンパク質の残存率を支配していると考えられる。
(4)蛍光色素の混合による分析の簡易化
カゼインナトリウムとタンニン酸の混合物に蛍光色素を混合すれば、タンパク質定量のような発色操作を行わなくても、色素を指標とした分光分析(吸光度測定)や蛍光検出法による簡便・迅速な定量が可能となる。この場合、洗浄前後でのタンパク質量と色素量の挙動が一致することが必須である。これまでに、筆者らはポリフェノール系色素であるクルクミンがカゼイン/タンニン酸と結合して水系の洗浄では除去されにくい複合汚れの構成成分として作用する現象を見出している。
図7に、クルクミンを混合したカゼインナトリウムとタンニン酸の混合物に対する水洗浄後の残存率を示す11)。残存量の評価は、拭き取り法とタンパク質定量法、拭き取り法とクルクミンを指標とする吸光光度法、そして紫外線照射時に発生する蛍光強度を測定する蛍光検出法(非接触)の3通りで行った。
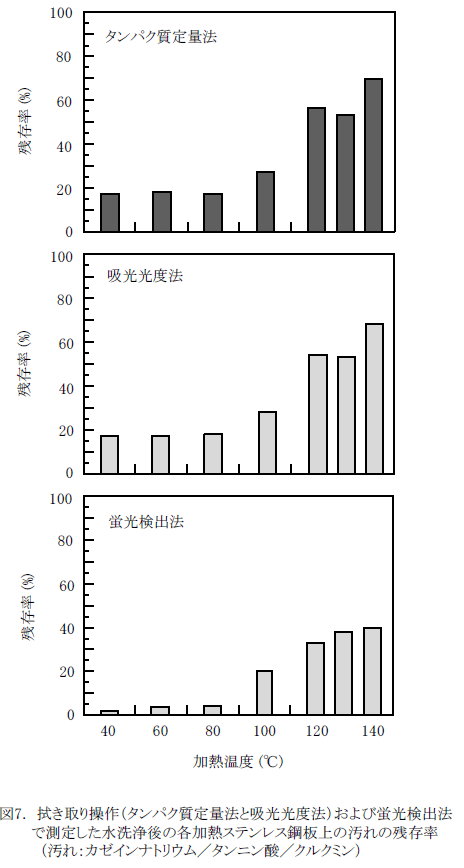
拭き取りとタンパク質定量で得られた残存率は、クルクミンの吸光度(470 nm)から算出した残存率と高い相関性が得られていることがわかる。ここでは示さないが、アルカリ剤や界面活性剤を用いた洗浄後の残存率においても、クルクミンを指標として残存率の定量的取り扱いが可能であることを確認している。クルクミン含有汚れを使用することで,煩雑なタンパク定量の代わりに,残存量を吸光度で簡便に測定できることは操作上の利点である。
また、蛍光検出法で測定した残存率は,拭き取り法で得られた値と比較すると相対的に低いが,残存率に及ぼす加熱温度の影響は一致していることがわかる11)。蛍光検出法は、表面の残留量を非接触方式で簡便に測定することができるため,残存量の評価工程の短縮かつ効率化につながると期待できる。
おわりに
ここで紹介した試験用汚れの調製法や拭き取り法および蛍光検出法による清浄度の定量化は、操作も簡便で、現場でも実施可能な試験内容である。いまだ検討すべき課題も残されているが、近い将来、食品製造機器の衛生構造(洗浄性)を自主検証するための試験法として普及するよう、業界の要望を取り入れながら鋭意開発を進めていく方針である。
参考文献
1) 大村宏之:防菌防黴,41, 275-281(2013).
2) European Hygienic Engineering & Design Group: Campden & Chorleywood Food Research Association Technology, Chipping Campden(2004).
3) 浦野博水,大村宏之,福崎智司:防菌防黴,38, 211-218(2010).
4) Lowry, O. H., Rosebrough, N. J., Farr, A. L., and Randall, R. J.: J. Biol. Chem.,
193, 265-275(1951).
5) 浦野博水,大村宏之,福崎智司:防菌防黴,43, 515-519(2015).
6) 浦野博水,大村宏之,福崎智司:防菌防黴,43, 313-315(2015).
7) Haslam, E.: Biochem. J., 139, 285-288(1974).
8) Takahashi, T., Nagai, T., Sakiyama, T., Nakanishi, K.: Food Sci. Technol. Int., 2, 116-119(1996).
9) Jeurnink, Th. J. M., Walstra, P., and de Kruif, C. G.: Neth. Milk Dairy J., 50,
407-426(1996).
10) 遊佐孝五 :日畜会報,27, 197-202(1956).
11) 幡野 玲,大萱宗一郎,浦野博水,髙橋和宏,大村宏之, 福崎智司:調理食品と技術,24,
in press(2018).
略歴
福崎 智司
三重大学大学院生物資源学研究科 教授
1991年3月広島大学大学院醗酵工学科博士課程後期修了後、同年4月岡山県工業技術センター入所。食品技術グループ長、研究開発部長を経て、2013年より現職。専門は、洗浄・殺菌工学、食品微生物学、生物化学工学、廃水処理工学。工学博士。
|









