| ◆ HOME >食品検査機関を取り巻くISOマネジメントシステムの動向-SUNATECでの変遷と統合- |
 |

食品検査機関を取り巻くISOマネジメントシステムの動向
-SUNATECでの変遷と統合-
 一般財団法人 食品分析開発センターSUNATEC 品質管理室
菊川浩史
SUNATECのマネジメントシステムの変遷
信頼性確保の第一歩は、組織のマネジメントシステムのあり方に他ならない。SUNATECのマネジメントシステムの変遷を表-1に示した。昭和54年(1979年)、地域の食品事業者向けに検査を始め、翌年に食品衛生法の旧指定検査機関として認可をいただいた。平成8年(1996年)に「指定検査機関における製品検査の業務管理要領」が通知され、指定検査機関に対しての要求事項が明確化された。続いて平成9年(1997年)に精度管理の一般ガイドラインが通知される。これら厚生労働省から発出される信頼性確保に関する通知に対応するかたちで、業務管理の整備を行ってきた。
一方、この頃から国際的な品質マネジメントシステムであるISO9001の導入が各企業で進み、SUNATECもISO9001(取得時はISO9002:1994)の導入を進めることとなった。そして、平成16年(2004年)に行われた指定検査機関から登録検査機関への移行を経て、ISO9001で組織運営を規定しながら、技術的要求事項は、「登録検査機関における製品検査の業務管理要領」に沿ってマネジメントシステムの構築を行った。その頃、ISO/IEC Guide25の改定と共に品質マネジメントシステムが組み込まれ、1999年にISO/IEC17025:1999として発行される。
また、平成19年(2007年)、前年開始された残留農薬のポジティブリスト化を起点とするように、以降、厚生労働省から試験法の妥当性評価法ガイドラインが順次通知され、信頼性確保のため、最難関課題であった試験法もしくは、試験所としての妥当性の確認・検証方法が明確なものとなっていった。
以上のような変遷を経て、平成20年(2008年)、検査受託機関にISO/IEC17025認定取得を意識せざるを得ない状況となり、また、SUNATECの素養を高める勉強機会としてISO/IEC17025:2005を取得した。
さらに平成21年(2009年)、食の健康志向が高まる中、健康増進法登録試験機関としての登録も受けた。
しかしながら、このような登録検査(試験)機関として、また試験所として、周辺環境の流れにあるがままに合わせた結果、登録検査(試験)機関としての要求事項、品質マネジメントシステムとしてのISO9001、試験所としての国際規格であるISO/IEC17025とそれぞれの要求事項に対して、点での対応を行い、製品検査(許可試験)は「業務管理要領」、一般受託検査は「ISO9001」、認定試験は「ISO/IEC17025」に分けた管理となり、トリプルスタンダードとなっていた。
表-1 SUNATECのマネジメントシステムの変遷
| |
変遷 |
特記事項 |
| 昭和54年(1979年) |
財団設立 |
|
| 昭和55年(1980年) |
食品衛生法指定検査機関 |
|
| 平成8年(1996年) |
|
指定検査機関における製品検査の業務管理要領の通知 |
| 平成9年(1997年) |
|
精度管理の一般ガイドライン通知 |
| 平成11年(1999年) |
|
ISO/IEC17025:1999規格制定
(ISO9001:1994を包括) |
| 平成13年(2001年) |
ISO9002:1994取得 |
|
| 平成16年(2004年) |
食品衛生法登録検査機関へ移行 |
|
| 平成17年(2005年) |
|
ISO/IEC17025:2005
(ISO9001:2000を包括せず) |
| 平成19年(2007年) |
|
妥当性評価ガイドライン(農薬) |
| 平成20年(2008年) |
ISO/IEC17025:2005認定取得 |
妥当性評価ガイドライン(金属) |
| 平成21年(2009年) |
健康増進法登録試験機関 |
|
| 平成26年(2014年) |
|
妥当性確認ガイドライン(有害物質) |
このようなトリプルスタンダード下では、当然、現場は混乱する。本来は検査技術の向上に邁進しなくてはいけない立場の検査員が、各マネジメント体系への対応のため集中力をそがれる結果となり、信頼性を確保するためのマネジメント体系が逆の効果を招きかねない状況となり得た。
登録検査機関
登録検査機関としての業務は「製品検査」(主に輸入食品の命令検査)であり、検査に対する疑義は即、国際問題となりうる。そのため、国際的にみて妥当な検査結果を得るために厚生労働省は登録検査機関に対して、各通知を発出した。その要求事項の概要は表-2の通りである。
表-2 登録検査機関としての業務の要求事項概要
| 項 |
概要 |
| 1.目的 |
製品検査の信頼性確保 |
| 2.組織 |
製品検査部門責任者、検査区分責任者、信頼性確保部門責任者、代表者の責任と業務 |
| 3.製品検査室等の管理 |
区画、環境整備 |
| 4.機械器具の管理 |
作業書の作成、適切な使用、点検管理 |
| 5.試薬等の管理 |
作業書の作成、適切な使用、管理 |
| 6.動物の管理 |
作業書の作成、適切な飼育、管理 |
| 7.有毒な又は有害な物質及び危険物の管理 |
法令順守、廃棄物の管理 |
| 8.試験品の取扱いの管理 |
サンプリング、移送、保管 |
| 9.製品検査の操作等の管理 |
作業書の作成、妥当性評価、試験法の最新版管理
※妥当性評価(確認)ガイドライン |
| 10.製品検査の結果の処理 |
結果の報告、確認手順と責任 |
| 11.製品検査結果通知書 |
報告様式の必要事項 |
| 12.試験品の保存 |
結果提出後の試験品保管 |
| 13.内部点検 |
実施手順 |
| 14.品質(精度)管理 |
内部品質管理の手順
※精度管理の一般ガイドライン |
| 15.外部品質(精度)管理調査 |
外部技能試験の手順 |
| 16.データの作成 |
記録の取り方 |
| 17.標本、データ等の保存 |
記録の保管方法、保管期間 |
| 18.研修 |
信頼性確保部門研修の受講、検査員への研修実施 |
| 19.外部査察 |
厚労省職員の立入り |
| 20.その他 |
苦情処理、不確かさ |
全国に100を超える食品衛生法に基づく登録検査機関があり、登録検査機関は「製品検査」に対して、これら要求事項を満たしている。ただし、登録検査機関の業態は様々である。公益財団(社団)法人、一般財団(社団)法人、株式会社などの法人の種類、また、食品検査を主とする機関の他、環境検査、臨床検査、医薬品検査を主とする機関、食品検査を主とする機関にあっても、栄養成分、微生物、残留農薬など主とする業務が違うなど、食品検査に対する各組織の立ち位置はまちまちである。更には、「製品検査」を主な業務としている機関から、ほぼ「製品検査」の実績が無い機関も実際には存在する。
このように一口に「登録検査機関」と言っても、その組織体を一様に示すものでない。まず前提として、「登録検査機関とは、政府の代行機関として、業務規程の認可を受けた製品検査を行うことができる検査機関のこと」であり、あくまで「認可を受けた製品検査」に対しての要求事項である。言い換えれば、この登録検査機関としての要求事項が機関組織全体へどのように組み入れられているかは、機関によって違うことを理解する必要がある。
ゆえに「登録検査機関」であるということが、その組織全体の「信頼性」を示せるものでは残念ながらない。しかし、「登録検査機関」を名乗る以上、全ての検査業務に対して、同等以上の管理が行われて然るべきである。
登録試験機関
登録試験機関は、健康増進法に基づく、特別用途食品(特定保健用食品を含む。)の許可試験(関与成分の定量試験)の実施機関で、独立行政法人国立健康・栄養研究所と登録試験機関が全国に5機関あるのみである。(http://www.caa.go.jp/foods/index4.html)
本年(H27年4月)開始された「機能性表示食品」の届け出において必要事項を取りまとめた「機能性表示食品の届出等に関するガイドライン」中に記載されている「登録試験機関」はこの機関のことである。
なお、登録試験機関における要求事項は、登録検査機関と基本的に同様であるため、「栄養成分分野」における「登録検査機関」と言い換えることが出来る。
ISO/IEC17025
ISO/IEC17025は、ISOと共にあるIECの頭文字が示す通り、この規格は国際電気標準と兼ねている。また、試験所及び校正機関を兼ねた規格でもある。電気・機械など、物理的試験のように、明確な「不確かさ」を求めることが出来る試験所においては、以前から「計測における不確かさの表現ガイド」(GUM : Guide to the Expression of Uncertainty in Measurement) に基づく「不確かさ」の解釈と理解は進んでいたが、こと食品分野の試験所における合理的な「不確かさ」の推定への理解は近年まで十分でなく、SUNATECが取得した平成20年(2008年)当時でもまだ、手探りだったと振り返ることが出来る。それゆえ、SUNATECが認定取得した試験法も実用的というよりは、認定審査指摘に容易に対応できるように簡易な試験法での認定となり、非常に恥ずかしい話であるが看板化していた。
しかし、初回認定から5年が経過し、厚生労働省から、妥当性評価(確認)の方法を示す通知も次々と発出され、試験法の妥当性確認の基準、試験所での検証基準も明確なものとなってきた。また、SUNATECでもISO/IEC17025の認定は主たる検査室である理化学2部門、微生物部門へと認定を拡大し、その価値観はおおよそ理解が出来てきた。(なお、ISO/IEC17025も登録検査機関での「認可された製品検査」と同様、対象食品と試験方法の組み合わせでの認定となるため、その組織全体の信頼性を示せるものではない。)
なお、組織全体が試験所であるSUNATECにおいて、信頼性確保に対して国際規格であるISO/IEC17025を中心に置く規格であることは疑う余地もない。
ISO/IEC17025と登録検査機関の要求事項
ISO/IEC17025の認定において最も特徴的なメリットは「ワンストップテスティング」である。ワンストップテスティングは、WTO/TBT協定(貿易の技術的障害に関する国際協定)によって、ISO/IEC17025の認定を受けた試験所の検査結果は、他のWTO加盟国で通用することである。
一方、登録検査機関が受け持っている「輸入食品の命令検査」の結果も輸出国が受け入れることが出来る検査結果でなくてはならず、そのため、厚生労働省は、登録検査機関に対して通知によって、業務管理要領などに基づく管理を義務づけてきたわけである。
高度成長期に日本の製造業の品質管理が、QC、TQC、TQMと発展し、国際化の中で、QMS(ISO9001)化と発展してきたのと同様、現在の登録検査機関に求められるのは、登録検査機関から、ISO/IEC17025認定試験所への脱皮であろう。厚生労働省の機関である横浜・神戸検疫所、検疫検査センターがISO/IEC17025の認定を受けたのもこの流れを肯定するものではないかと考えている。
また、現在の食を取り巻く国際的な状況(環太平洋戦略的経済連携協定[TPP]や、国際的な日本の食品ブーム)を鑑みたとき、食品検査受託機関としてISO/IEC17025の認定は必須ともいえる。
ISO/IEC17025の要求事項と登録検査機関としての要求事項の相関を、表-3に示した。
表-3 ISO/IEC17025と登録検査機関の要求事項対比表
| ISO/IEC17025要求事項 |
業務管理要領の要求事項
(※は他通知等から引用 |
| 4.管理上の要求事項 |
|
| 4.1組織 |
2組織
7.有毒な又は有害な物質及び危険物の管理 |
| 4.2マネジメントシステム |
- |
| 4.3文書管理 |
(別添) |
| 4.4依頼、見積もり仕様書及び契約内容の確認 |
※食品衛生法施行規則第7章など |
| 4.5試験の下請負契約 |
- |
| 4.6サービス及び供給品の購買 |
5.試薬等の管理(6.動物の管理) |
| 4.7顧客へのサービス |
- |
| 4.8苦情 |
20.その他(3)苦情等の処理 |
| 4.9不適合の試験業務の管理 |
13.内部点検
14.品質(精度)管理
15.外部品質(精度)管理 |
| 4.10改善 |
- |
| 4.11是正処置 |
13.内部点検
14.品質(精度)管理
15.外部品質(精度)管理 |
| 4.12予防処置 |
|
| 4.13記録の管理 |
16.データの作成
17.標本、データ等の保存 |
| 4.14内部監査 |
13.内部点検 |
| 4.15マネジメントレビュー |
- |
| 5.技術的要求事項 |
|
| 5.1一般 |
- |
| 5.2要員 |
18.研修 |
| 5.3施設及び環境条件 |
3.製品検査室等の管理 |
| 5.4試験の方法及び試験の妥当性 |
9.製品検査の操作等の管理
20.その他(4)不確かさの評価
※各試験法(分析法)の妥当性評価(確認)ガイドライン |
| 5.5設備 |
4.機械器具の管理 |
| 5.6測定のトレーサビリティー |
5.試薬等の管理(6.動物の管理) |
| 5.7サンプリング |
|
| 5.8試験品目の取り扱い |
8.試験品の取り扱いの管理
12.試験品の保存 |
| 5.9試験の品質の保証 |
10.製品検査の結果の処理
14.品質(精度)管理
15.外部品質(精度)管理
※品質(精度)管理の一般ガイドライン |
| 5.10結果の報告 |
11.製品検査結果通知書 |
| その他 |
|
| 認定審査、維持審査 |
19.外部査察 |
このように、登録検査機関としての要求事項を満たす運用が出来ていれば、技術的な観点を中心に、ほぼISO/IEC17025の要求事項を満たすことが分かる。
一方で、マネジメントシステムのレビュー部分で補完が必要なことが垣間見られる。
このことは、ISOが最も重視するPDCAを意識することで補完可能である。ISOが組織のあらゆる情報源からシステムのレビューを行い、PDCAを回す仕組みにあるのに対し、登録検査機関のPDCAは、各責任者を中心とした組織のマネジメント層の意識にゆだねられる傾向が強い。よって、組織マネジメント層と現場の乖離が起こっているような組織はその信頼性が非常に脆弱になる可能性がある。時折起こる登録検査機関の不祥事はこのような事由も関与しているともいえる。(マネジメントシステムのレビュー機会は、厚生労働省による査察に頼ることになりかねない。)
そうであるのなら、この国際問題に発展しかねない登録検査機関としての要求事項は、早々にISO/IEC17025に置き換えるべきとも言える。そこでSUNATECは、登録検査機関の業務として、製品検査の認可と、ISO/IEC17025の認定とを統合する方向での取り組みを開始することとした。
ISO9001
ISO9001の要求事項は、細かな用語や要求事項の違いはあるが、根本的には、ISO/IEC17025の管理的要求事項と同質である。よって、組織全体が試験所であるSUNATECでは基本的にダブルの「品質マニュアル」は必要はない。
マネジメントシステムの有るべき姿
図-1にSUNATECが目指すマネジメントシステムの有るべき姿を示した。従前、ISO9001をベースに構築したマネジメントシステムを払拭し、ISO/IEC17025第4章:管理的要求事項を主として再構築を行い、ISO9001とのダブル品質マニュアル化を解消した。また、製品検査(許可試験)は、ISO/IEC17025の要求事項と統合を果たし、運用ルールを一元化した。これらにより、無駄が排除され、内部技能試験、外部技能試験、内部監査(内部点検)、認定維持審査(厚生労働省査察)など、全て同じ記録類での運用が可能となった。統合された運用はミスの削減、混乱の除去が見込め、このマネジメントシステムの「統合」により信頼性の確保につながると確信している。
なお、ISO/IEC17025認定以外の検査業務は、必要に応じていつでも認定可能な状況に置いておくことで、組織全体の信頼性を獲得する所存である。
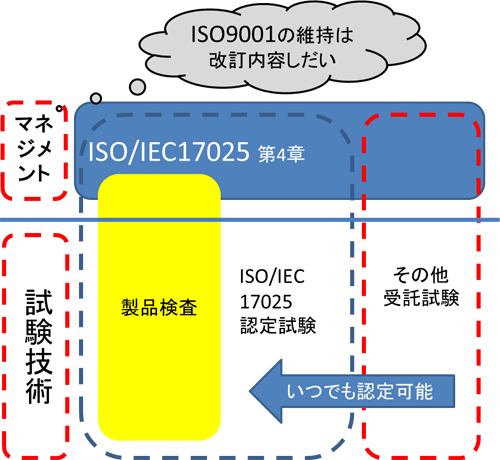
図-1 SUNATECマネジメントシステムの有るべき姿
|


