|
食品工場の微生物制御への有機酸の利用技術
食品・微生物研究所 所長 内藤茂三
1.はじめに食品添加物としての有機酸、例えばソルビン酸、プロピオン酸、安息香酸などの酸性保存料の効果はpHにより著しく異なり、低pHほど抗菌力が増大して微生物が容易に殺菌できる。これは有機酸の解離度がpHにより変化するためで、pHが低下して水素イオン濃度が増加すると解離は抑制され、非解離分子の割合が多くなる。非解離分子は解離した分子よりも細胞膜透過性が大きいために強い抗菌力を示すようになる。このため有機酸の使用技術は濃度ではなくpHが重要であると言われてきた。また対象微生物により有機酸の効果が異なることも指摘されてきた。最近ではpH4.9の酸性下で0.25%のソルビン酸、プロピオン酸を資化する酵母や酢酸を資化するカビが出現して食品の変敗の原因となっている。
2. 有機酸の抗菌性
酢酸、乳酸、クエン酸を初めとする有機酸には食品の変敗を防止する作用のあることが古くから知られてきた。有機酸の抗菌性はpH低下によるものと、解離していない有機酸の比率(非解離型が殺菌力が強い)、有機酸自身の有する抗菌力とによるものとがある。pH低下は酸性保存料であるソルビン酸のように、酸の非解離型分子の比率が増加して細胞膜を通過し易くなり、抗菌力が高まる。細胞内での代謝による水素イオン濃度の増加に伴う、細胞液の酸性化による核タンパク質の変性に起因する。
脂肪族有機酸の抗菌性をpH変化による非解離分子の影響を除去して比較するために各有機酸を0〜0.5%の範囲に添加後、pHを全て5.0に調整して検討した結果、B.megaterium に対する抗菌効果は酢酸>乳酸・コハク酸>リンゴ酸>酒石酸・クエン酸> 塩酸の順で、酢酸が著しく強いのに対しリンゴ酸以下は微弱であり、塩酸はほとんど認められない。この抗菌力の強さはpH5.0における各有機酸の非解離型分子の濃度比率の大小とよく一致しており、解離恒数の小さいものほど抗菌性が強い。 腐敗及び変敗細菌の生育抑制効果を検討した結果、pH5.0における抗菌力は酢酸が最も強く、次いでコハク酸、乳酸の順であり、グラム陰性細菌やグラム陽性細菌に効果がある。 有機酸と同様にソルビン酸、プロピオン酸、安息香酸等の酸性防腐剤や次亜塩素酸ナトリウム等の殺菌剤は低pH域で抗菌力や酸菌力が大きい。 クエン酸はグラム陽性細菌に抗菌活性を持ち、肉製品の冷却期間における他の微生物の制御に利用されている。酢酸は、食塩と組み合わせることによって、グラム陰性細菌に対し抗菌効果がある。有機酸の抗菌効果を評価するには各有機酸の塩基当量を考慮し、有機酸の塩基当量が小さいものは少量の有機酸でpHを低下させる。フマル酸は、食用可能な塩基当量の最も小さい有機酸(塩基当量58)で少ない量でpHを低下させることができ、グラム陰性菌に0.1〜0.3%で抗菌効果を示す。その他の有機酸の塩基当量は酢酸、乳酸、クエン酸、リンゴ酸、コハク酸でそれぞれ60、90、64、67、59である。 有機酸によるサルモネラが増殖する最低のpHを表1に示した 表1 有機酸によるサルモネラ増殖最低pH
3.有機酸の抗菌機構
非解離状態で微生物の菌体内部に侵入した有機酸が菌体内のpHにより解離され菌体内のpHを低下させ酵素等が障害を受けて修復不可能な状態によって起こる。この機構はそれぞれの有機酸の微生物菌体への付着性、細胞膜透過性、有機酸の親水性、有機酸の疎水性によって影響を受ける。有機酸は解離した状態ではイオンの形となり微生物菌体の表面に吸着する。非解離状態では細胞膜を透過して菌体内に容易に侵入する。つまり解離している酸は菌体内に侵入せず(アルカリ側)非解離の有機酸は菌体内に侵入(酸性側)する。
菌体内に侵入した非解離型有機酸は解離してプロトンが生成する。菌体内のpHが低下し、酵素が不活化し、死滅する。細胞内のプロトンを排除するのにエネルギー消費し増殖が遅れる。 有機酸はそれぞれ固有の解離定数を有し、解離定数により非解離状態が予測できる。弱酸は強酸より非解離分子が多いので抗菌作用は強い。有機酸の解離状態はpHにより影響され、弱酸は高いpHでよく解離し、強酸は低いpHでよく解離する。各有機酸が半分解離したpHをpKaといい、表2にとりまとめた。 水中で電離する化合物の酸性の強弱は、その物質の電離度によっておおまかに分類される。電離度は電解質が溶液中で解離(電離)しているモル比をあらわす値で、電離度がほぼ 1 である酸を強酸、電離度が小さいものを弱酸と呼ぶ。また、純硫酸よりも強い酸性媒体を超酸という。より定量的に酸の強さを示す場合は、解離平衡を考え、その平衡定数 Kaの対数に負号をつけた解離定数pKaで表す。塩基に対しては、共役酸の pKa、特に水中の場合では塩基性度定数 pKb = 14 − pKa が用いられる。例えば、酢酸の pKa は 4.76 、ギ酸の pKa は 3.77 である。pKa は定義から数値が小さいほど水素イオンを解離しやすい、すなわち強い酸であることを示す。したがって、同じ弱酸でもギ酸のほうが酢酸より 10 倍強いことが分かる。酸は強酸とか弱酸に分類するが定量的でない。 pKaはそれを定量的に示すため解離度を使用する。 HAなる酸がH+とA−に解離し、 HA=H+ + A− 解離定数(Ka) = [H+][A−] / [HA] pKa=−logKa 解離度大きい塩酸は未解離の「HA]が小さく、 [H+][A−]が増え、Kaは大きくなり、 pKaは小さくなる。解離度の小さい酸ほどpKaは大きくなる。 pKa1は多価の酸の第1解離、pKa2は第2解離、pKa3は第3解離を表す。 表2 水溶液中での有機酸の解離定数(pKa)
いずれの有機酸もpHが低下するほど非解離型分子の割合が増加するので低pHほど抗菌力は強くなる。有機酸の解離は溶液のpHが高ければ大きく逆にpHが低ければ解離が抑制される。 それぞれの有機酸についてpHと解離度の関係は定まっている。酢酸は低いpHでも解離の度合いは小さく、pH4では80%が、pH5でも40%が解離しない状態である。このため酢酸は微生物の増殖抑制に高い効果を持っている。酢酸は水溶液の中で解離し、マイナスに荷電した有機酸のイオンとプラスの水素イオンとに分かH+れる。
細菌の表面の膜を構成している脂質二重層は、外からのイオンの侵入に対して防壁となる。イオンは細胞の中には侵入できない。解離しない形の有機酸は脂質二重層を通って細胞内に侵入し細胞内の水素イオン濃度を高め、pHが低下する。 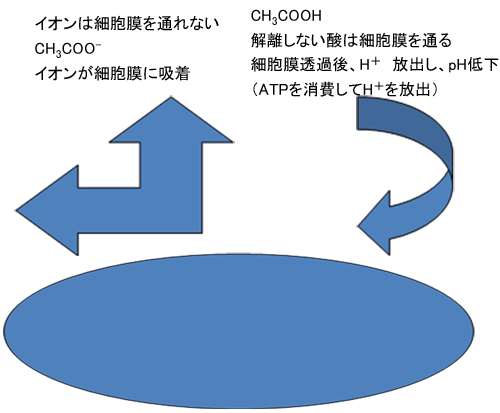
4.有機酸と緩衝液の抗菌性
有機酸によって、食品の保存性を高めようとする場合、食品そのものの緩衝力が弱いものや、抗菌作用を高めるため有機酸を多量に添加したいもの、食品風味の淡泊なもの、ある有機酸の酸味をできるだけ抑えて使用したい場合などにおいて、直接有機酸のみを使用すると添加量のバラツキによるpHの変動や香味への影響等により的確にできない。このような場合、抗菌力に優れた有機酸を緩衝液の型にして使用すれば有機酸の添加量も自由に変化させることができ、また各有機酸の微生物制御可能な特徴を生かした使用方法ができる。また現在の食品変敗主原因菌である乳酸菌の有機酸による制御ではpH5以下の酸性域では乳酸より酢酸の方が抗菌効果が高い。pH6〜7では酢酸より乳酸の方が抗菌効果が高い。クエン酸はpH5以下の酸性域では抗菌効果を示さず、pH6〜7の中性域で抗菌効果を示す。乳酸やアジピン酸は乳酸菌には効果を示す真菌(カビや酵母)には抗菌効果を示さない。バチルス菌の有機酸による制御では酢酸>アジピン酸>コハク酸>乳酸>リンゴ酸>クエン酸>酒石酸>塩酸となる。Bacillus polymyxa はpH5以下で酢酸と乳酸に増殖抑制効果があり、 Bacillus coagulans はpH5以下でフマル酸、酢酸、クエン酸に増殖抑制効果がある。酢酸の殺菌効果の特徴を表3に、緩衝液のpH範囲を表4に示した。
表3 酢酸の殺菌効果の特徴 1.0.1%で多くの食中毒菌の生育抑制 2.2.5%以上で多くの細菌の殺菌 3.酵母、乳酸菌は2.5%でも生育する。 4.酢酸濃度が高いほど抗菌効果が高くなる。 5.酢酸と食塩を併用することで抗菌効果高まる。 6.温度を上げることによって抗菌効果高まる 表4 緩衝液のpH範囲
酢酸緩衝液の保存効果では酢酸ナトリウム(無水、結晶)、二酢酸ナトリウム(酢酸と酢酸ナトリウムを結合させたもの)でpH4.80 、食塩11.7%での結果を示す。 食塩のみでは殆どの酵母が生育し、食塩存在下での酢酸緩衝液の酵母抑制効果が認められた。酢酸緩衝液0.1Mでは抑制効果は殆どなく、酢酸緩衝液0.2Mで一部の酵母が抑制された。酢酸緩衝液0.3MでCandida etchellsii以外の酵母が抑制され、酢酸緩衝液0.5Mで全ての酵母が抑制された。抑制効果のある酵母(pH4.80,食塩11.7%, 30℃、13日後)は酢酸緩衝液0.2Mでは Sacchaomyces baynus 、Saccharomyces carlsbergensis 、Candida famata ,Debaryomyces hansenii であった。酢酸濃度0.3M ではCandida属(Candida etchellsii以外)全て の酵母であった。 5. 有機酸塩の抗菌性
いかの燻製製造工場で製造されたいかの燻製に白色粘凋物質が生成、その原因菌は耐塩性のMicrococcus属細菌であった。2種類のMicrococcus属細菌であることが同定された。これらの細菌の増殖を防止するために有機酸塩の検討を行った。
分離・同定したいかの燻製の白色粘凋物質原因菌のそのうちの1種耐塩性細菌Paracoccus halodenitrificansに対する有機酸塩8種類、リンゴ酸ナトリウム、クエン酸ナトリウム、酢酸ナトリウム、コハク酸ナトリウム、ギ酸ナトリウム、フマル酸1ナトリウム、クエン酸カリウム、酢酸カリウムの増殖に及ぼす影響について検討した結果を図2に示した。 顕著に増殖抑制効果が認められたのはクエン酸ナトリウムであり、2%添加ではやや増殖するが4%以上添加すると完全に抑制可能であった。またクエン酸カリウムでは6%以上の添加で完全に抑制された。リンゴ酸ナトリウムは2〜6%の添加では増殖を促進したが、10%添加でほぼ完全に増殖が抑制された。コハク酸ナトリウムは2〜10%添加により増殖を促進した。また酢酸ナトリウム、酢酸カリウム、酢酸カリウムの添加により菌の増殖抑制効果は認められなかった。なおフマル酸1ナトリウムは2〜10%添加により添加直後よりpHが3.4〜3.6と低下したため菌は増殖不能であった。 一般的に菌の増殖は2〜10%有機酸塩の添加により初発pHは6.0〜7.0(フマル酸第1ナトリウムを除く)で、30℃、10日間培養でpHは6.6〜8.3に著しく変化した。増殖抑制効果が最も顕著であったクエン酸ナトリウムを2〜10%添加直後のpHは6.6〜7.0であったが30℃、10日間培養後のpHはほとんど変化しなかった。酢酸ナトリムを2〜10%添加直後のpHは6.4であったが30℃、10日間培養後はやや6.6〜7.0と上昇した。なお有機酸塩無添加の場合、培養開始前はpH7.0であったが、30℃、10日間培養後pH5.4〜5.8に低下した。
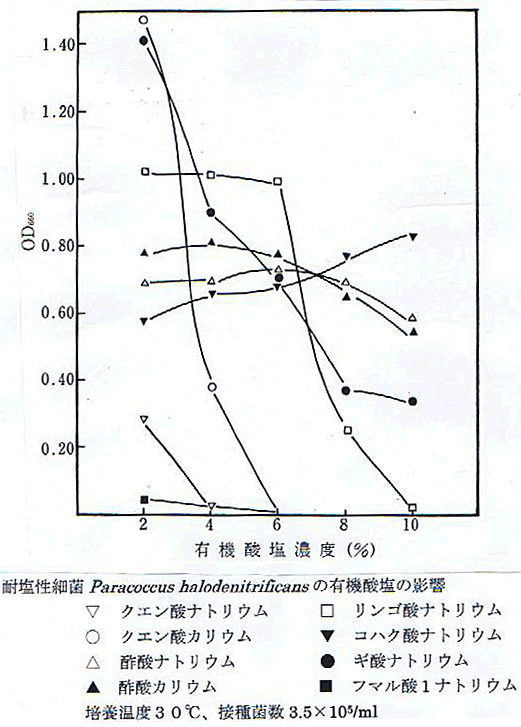 図2 いかの燻製の白色粘凋物質原因菌である耐塩性細菌Paracoccus halodenitrificansに対する有機酸塩の増殖に及ぼす影響 サナテックメールマガジンへのご意見・ご感想を〈e-magazine@mac.or.jp〉までお寄せください。 |
| Copyright (C) Food Analysis Technology Center SUNATEC. All Rights Reserved. |

